Термин неметаллические полезные ископаемые в некоторой степени двусмыслен: он не является ни строго научным, ни точным экономическим термином. Однако им широко пользуются, и он охватывает группу полезных ископаемых, которые добываются для других целей, нежели получение металлов, в них содержащихся. Неметаллические полезные ископаемые удобно классифицировать не на основе распространенности в земной коре элементов, входящих в их состав, а по областям применения. Во-первых, здесь можно выделить полезные ископаемые, в основном используемые для агрохимических целей, главным образом в виде удобрений и в качестве сырья для химической промышленности. Эти виды сырья составляют 33 % от объема добычи неметаллических полезных ископаемых. Во-вторых, выделяются материалы для строительства и строительной промышленности.
Полезные ископаемые для производства удобрений
Месторождения сырья для производства удобрений, несомненно, являются одним из самых насущных ресурсов, без которых невозможно увеличение производства продуктов питания для удовлетворения потребностей растущего населения Земли, стремящегося к улучшению своего жизненного уровня. Растению для роста требуется много химических элементов. Кислород и водород (извлекаемые из воды) вместе с углеродом (извлекаемым из двуокиси углерода атмосферы) составляют 98 % основной массы живых растений, однако азот, фосфор, калий, кальций и сера им столь же необходимы. Растения суши — источник наших пищевых запасов — извлекают эти элементы из почвы. Уровень их содержания во многом определяет скорость роста растений. Чтобы элементы могли оказывать влияние на рост, они должны находиться в почве в хорошо усваиваемой растениями форме. Например, в большинстве почв калия содержится более 1 %, но подавляющая его часть недоступна для растений, так как он заключен в нерастворимых силикатах типа полевых шпатов. Для повышения скорости роста растений калий вносится в почву обычно в виде сульфата K2SO4 или хлорида KCl, потому что оба эти соединения легкорастворимы. Действенность азотных, фосфорных и других удобрений также зависит от их растворимости, поэтому к ресурсам удобрений относятся растворимые соединения или минералы, которые после обработки легко превращаются в растворимые разновидности. Геологи ведут поиск именно таких ресурсов удобрений.
Наиболее важные удобрения — «большая троица» — фосфорные, калийные и азотные. Они вносятся в почву в отношении примерно 1 : 1,5 : 3, но при этом следует помнить, что удобрения применяются не в виде химических элементов, а в виде различного рода соединений, которые все чаще называют компаундами. Потребности в удобрениях быстро увеличиваются, а их мировое потребление удваивается каждые десять лет. Спрос на удобрения едва ли будет уменьшаться, так как население земного шара продолжает расти. Наибольшие темпы роста в использовании удобрений отмечаются сейчас в таких странах, как Бразилия, где большие площади бедных почв вовлекаются в сельскохозяйственный оборот. Запасы главных элементов удобрений, к счастью, очень велики.
Азот. Азот — главный ресурс, извлекаемый из атмосферы. Форма, в которой он вносится в почву, — это различные растворимые нитраты, такие, как NaNO3, или компаунды аммония, такие, как (NH4)2SO4 и NH4NO3.
Большинство искусственных соединений азота получаются с помощью различных вариантов процесса Габера — Боша, в ходе которого атмосферный азот и водород (обычно в форме метана СН4 из природного газа) соединяются при высоких температурах и давлениях с образованием аммиака, или как побочный продукт в коксовых печах. Процесс требует большого количества энергии; заводы по производству азотных удобрений являются одним из самых энерго- и капиталоемких промышленных предприятий. Тем не менее на азот приходится наибольшая доля в мировом потреблении удобрений. Стоимость последних строго зависит от стоимости затраченной энергии. Атмосферный азот является главным источником для азотистых компаундов, хотя в небольших количествах продолжают добываться природные нитраты на чилийских месторождениях. Нитраты относятся к хорошо растворимым солям, но в почвах пустыни Атакама (Чили), где фактически нет дождей, они все же накапливаются. Интересно историческое замечание. В так называемой Тихой войне 1879—1883 гг. Чили сражалась против Боливии и Перу за контроль над месторождениями нитратов в пустыне Атакама, однако с открытием процесса Габера — Боша эти месторождения утратили свое значение.
Почти 20 % ежегодно потребляемого азота производятся в Соединенных Штатах Америки и половина — лишь в четырех странах.
Калий. Калий является широко распространенным элементом, подавляющая часть которого заключена в практически нерастворимых силикатных минералах. В качестве удобрений используются растворимые минералы калия, встречающиеся исключительно в месторождениях, известных как морские эвапориты, которые образуются в результате накопления солей при испарении морской воды. С морскими эвапоритами связано производство и других полезных компонентов, поэтому рассмотрим кратко их происхождение.

Главные компоненты морской воды
Основные элементы, растворенные в морской воде, могут переходить в соединения, которые осаждаются из морской воды, сохраняя равновесие между положительным зарядом катионов (Na+ 1) и отрицательным зарядом анионов (Cl-1), чтобы не нарушить электрическую нейтральность раствора и осажденных солей. Хлорид натрия — резко преобладающий компонент среди растворенных веществ; далее следуют соли магния, сульфат кальция и хлорид калия. Когда вода испаряется, концентрации в рассоле возрастают, и в конце концов достигается насыщение раствора сначала одной солью, потом другими. Отнюдь не всегда в первую очередь выпадает вещество, содержащееся в наибольших количествах. Насыщение сравнительно малорастворимым, а потому и находящимся в меньшем количестве в растворе компонентом обычно достигается задолго до насыщения хорошо растворимыми компонентами.
Первым компонентом, который осаждается при испарении морской воды, является СаСОз; его растворимость необычайно низка, а количество в растворе мало по сравнению с NaCl. Следующий компонент — CaSO4 не осаждается до тех пор, пока раствор не сократится до 19 % своего первоначального объема.
В зависимости от температуры может осаждаться либо CaSO4, либо CaSO42H2O.
NaCl — третий компонент — начинает осаждаться после того, как остаточный раствор достигнет 9,5 % исходного объема. Осаждение NaCl и небольшого количества CaSO4 продолжается до тех пор, пока рассол не сократится до 4 % своего первоначального объема. После этого начинает осаждаться первый компонент, содержащий магний и калий,— сложная соль, называемая полигалитом K2SO4 ∙ MgSO4 ∙ 2CaSO4 ∙ 2H2O. Сначала количество NaCl в растворе велико, и значительно больше половины его осаждается, пока объем раствора не сократится с 9,5 до 4 %. Следовательно, самым мощным слоем, образовавшимся в течение единичного цикла испарения, будет слой NaCl. Последовательность минералов, выделяющихся из оставшихся 4 % рассола (называемых «горькими солями»), сложна, разнообразна и зависит как от температуры, так и от того, контактирует или нет с ранее отложенными солями оставшаяся жидкость и, следовательно, возможно ли ее взаимодействие с ранее образованными кристаллами. Двумя осаждающимися солями, встречающимися в большинстве эвапоритовых толщ, являются сильвин КС1 и карналлит KCl∙MgCl2 ∙ 6Н2О; именно в этих минералах поздних стадий испарения заключена основная часть используемых мировых ресурсов калия.
Последовательность осаждения солей и их объемы, образующиеся при испарении изолированного объема морской воды, показаны на рисунке.
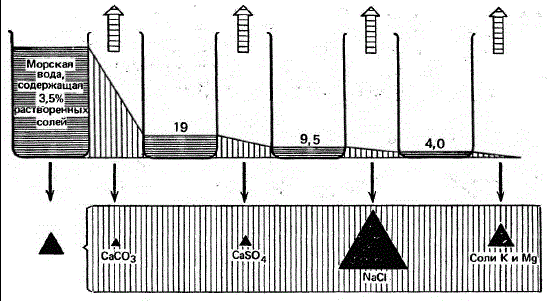
Последовательность осаждения соединений из морской воды. Когда в результате испарения начальный объем воды сократится до 19 %, начинается осаждаться CaSO4 когда до 9,5 % — NaCl, и т. д.
Однако в природных отложениях эвапоритов такие соотношения солей обнаруживаются редко. Образующиеся на первой стадии осадки СаСО3 и CaSO4, как правило, более обильны, а отложения солей К и Mg, осаждающиеся позже, встречаются несколько реже. При полном испарении морской воды в бассейне с глубиной Средиземного моря (в среднем 1370 м) образовались бы только 24 м NaCl и слой CaSO4 мощностью 1,4 м. Однако нередки пласты CaSO4 и NaCl мощностью в несколько сот метров. Результаты изучения окаменелостей в ассоциирующихся с солями осадочных породах позволили сделать вывод, что испарение происходило в мелких морских бассейнах. Ясно, что должен существовать иной механизм, нежели простое высыхание изолированного мелкого бассейна. Общим условием следует считать осаждение в отчасти изолированном бассейне, из которого вода удаляется при испарении, но который и непрерывно пополняется новыми порциями морской воды. Такой режим может иметь место в ряде геологических обстановок. Обобщенно они называются замкнутыми бассейнами. В такие бассейны вода поступает через полусливной бар. Испарение поверхностных вод приводит ко все более высокой концентрации растворенных солей в бассейне, так как рассол благодаря своей большей плотности постепенно опускается на дно.
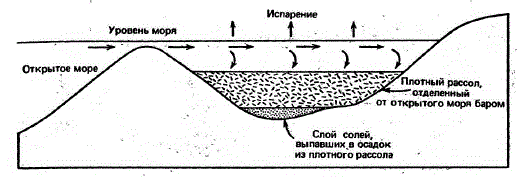
Схематическое поперечное сечение ограниченного бассейна. Свежая морская вода поступает через бар и в процессе испарения Концентрация солей в ней повышается. Плотный рассол опускается на дно, а бар препятствует его возвращению в открытое море. Когда рассол достигает определенной солености, соли осаждаются и могут в конечном счете заполнить бассейн.
Ограничивающий бар препятствует перемешиванию воды. Соленость бассейна увеличивается медленнее, чем это наблюдается при непосредственном испарении изолированного объема морской воды, а соленость рассола длительное время остается на уровне осаждения СаСО3. Вполне возможно, что выпадающий в осадок СаСО3 заполнит бассейн до уровня бара, прежде чем соленость достигнет величины, при которой начнет осаждаться CaSO4. Аналогичным образом могут сформироваться мощные залежи CaSO4, и рассолы никогда не смогут достичь стадии осаждения NaCl. Частота встречаемости эвапоритовых солей и их суммарная мощность в осадочных бассейнах повсеместно уменьшаются в последовательности: СаCO3 > CaSO4 > NaCl > соли К и Mg.
В настоящее время эвапоритовые отложения формируются на всех континентах. Хотя высокие температуры не обязательны для концентрации солей — суховеи могут выполнять те же функции и в холодном климате, — большинство эвапоритов образуются все же в поясе 35° с. ш. — 35° ю. ш. Все современные месторождения невелики по масштабам и в настоящее время на планете нет окраинных морей с ограниченными течениями и по размерам близких к Балтийскому, Средиземному или Черному морям, для которых выполнялись бы одновременно и морфологические, и климатические условия, необходимые для образования крупного месторождения эвапоритов. На сегодняшний день наибольшим, вероятно, является залив Кара-Богаз-Гол (СССР) на восточной окраине Каспийского моря. Однако если мы обратимся к геологической летописи, то обнаружим, что это временная ситуация, так как эвапориты широко развиты и в пространстве и во времени, а в прошлом неоднократно и почти повсеместно создавались условия, гораздо более подходящие для формирования морских эвапоритов, чем это наблюдается в настоящее время. В пермский период были сформированы исключительно мощные толщи эвапоритов в Северной Америке и в Европе. К тому же и само слово пермский произошло от пермского бассейна в СССР, к которому приурочено одно из крупнейших в мире месторождений эвапоритов.
Эвапориты являются главным источником галита (NaCl известен как обычная поваренная соль), гипса CaSO4∙2H2O и солей калия. В некоторых случаях в качестве побочных продуктов получают магний и другие менее распространенные элементы. Галит и гипс мы рассмотрим позднее, а здесь сосредоточим наше внимание на соединениях калия.
Многие годы спрос на калийные удобрения удовлетворялся за счет обширных пермских месторождений эвапоритов в Германии. По иронии судьбы в годы первой мировой войны США остались без нужного им сырья, ибо месторождения Германии оказались для них недоступны. Это обстоятельство стимулировало поиск и открытие новых, даже более богатых месторождений того же возраста и типа в штате Нью-Мексико. Здесь в пермскую эпоху в обширном, но мелком море сформировалась мощная толща эвапоритовых солей на площади не менее 160 тыс. км2; на ней теперь располагаются штаты Нью-Мексико, Техас, Оклахома и Канзас. На одном из участков этого бассейна (около Карлсбада, штат Нью-Мексико) на площади, в 4,8 тыс. км2 обнаружены пласты солей калия, мощность которых достигает 4 м. Эти месторождения являются наиболее богатыми в мире, хотя они невелики по сравнению с другими месторождениями. Запасы и потенциальные ресурсы калия составляют здесь примерно 100 млн. т.
Кроме указанных Северная Америка располагает еще рядом крупных месторождений калийных солей. Так, бассейн пенсильванского возраста в юго-восточной части штата Юта и в юго-западной части штата Колорадо — так называемый бассейн Парадокс — содержит богатые калием соли, площадь развития которых составляет 12,6 тыс. км2. Хотя значительная часть пластов солей калия залегает здесь слишком глубоко для рентабельной разработки, некоторое количество солей извлекается уже сейчас с помощью буровых скважин методом растворения солей непосредственно под землей, откуда растворы выкачиваются, а соли калия отделяются при выпаривании раствора на поверхности.
В провинции Саскачеван (Канада) и в ближайших к ней штатах США (Северная Дакота и Монтана) открыты, но пока еще недостаточно разведаны огромные запасы калийных солей в бассейнах Элк-Пойнт и Уиллистон девонского возраста. Согласно опубликованным данным, 37 500 млн. т. калийных солей доступны для современных методов разработки. Это крупнейшие из известных на Земле ресурсы, однако большими ресурсами располагает также СССР, а в последние годы крупные месторождения открыты в таких далеко отстоящих друг от друга регионах, как Южная Америка и Юго-Восточная Азия. Единственные континенты, где пока еще не обнаружены эвапориты с калием, — это Австралия и Антарктида. Кроме того, почти неисчерпаемым потенциальным ресурсом являются соли, растворенные в морской воде, поэтому даже больший по сравнению с современным спрос на калийные удобрения не должен вызвать серьезных трудностей.
Фосфор. Круговорот фосфора относится, по-видимому, к одному из самых нарушенных в результате интенсивной культивации земель. Фосфор является жизненно важным элементом для многих процессов, происходящих в клетках человеческого тела. Основная его часть сосредоточена в скелетах, состоящих из апатита Ca5(PO4)3(ОН), и после нашей смерти этот запас фосфора уже не возвращается в почвы. Следовательно, его нужно возмещать, т. е. вносить удобрения. Единственным источником фосфора и единственным распространенным минералом фосфора является апатит, но он слаборастворим. В связи с этим в обычной практике апатит (или фосфатные породы, как называют большую часть сырья, богатого апатитом) приходится обрабатывать разбавленными кислотами, чаще всего серной кислотой H2SO4, чтобы превратить апатит в более растворимое вещество. Химические реакции, которые происходят, когда серная кислота реагирует с апатитом, очень сложные; получающийся при этом суперфосфат отличается высоким содержанием такого растворимого в воде компаунда, как Ca(H2PO4)2.
В небольших количествах апатит встречается во многих горных породах, независимо от того, являются они изверженными, метаморфическими или осадочными. Большие концентрации апатита иногда устанавливаются в изверженных породах, но такие случаи относительно редки. Подобное скопление апатита известно на Кольском полуострове, на севере Советского Союза, в породах, называемых сиенитами, которые разрабатываются из-за содержащегося в них апатита и являются главным источником советских фосфорных удобрений. Есть еще одна разновидность изверженных горных пород — карбонатиты, которые служат источником как апатита, так и ниобия. Такие месторождения известны в Бразилии и в ЮАР — крупное интрузивное тело Палабора. Однако и большая, часть современной мировой добычи, и почти все известные запасы связаны с морскими, осадочными месторождениями апатита. В настоящее время они обеспечивают примерно 82 % мирового потребления фосфора, остальное приходится на изверженные горные породы (16%) и на гуано (2 %), которое представляет собой разложившийся в условиях сухого климата помет морских птиц.
Вопрос о происхождении морских фосфатных отложений окончательно не решен, однако общая картина их формирования уже понятна, поскольку осаждение апатита наблюдается сегодня в зоне апвеллинга, где холодные, обогащенные фосфором воды поднимаются из океанских глубин. Если это происходит вдоль мелкого континентального шельфа или в бассейнах с ограниченным водообменом, насыщение морской воды апатитом и последующее его осаждение могут быть вызваны рядом факторов. Например, почти лишенные кислорода или бескислородные воды создают среду с менее щелочным составом воды, в которой растворимость апатита понижается и он осаждается. Такие обстановки необычны в море, особенно в больших масштабах, однако, когда они все-таки возникают, как, например, в бассейнах с ограниченным притоком воды, для накопления фосфатных осадков необходимо такое расположение бассейна, чтобы привнос обломочного материала был незначительным, иначе будет происходить разбавление медленно осаждающегося фосфата. На территории современного Запада США апвеллинг определенно имел место в перми.
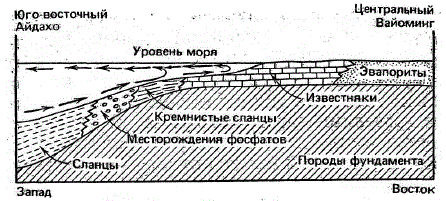
Схематическое изображение отложения апатита в формации Фосфория в западной части США
Образованные таким образом пласты особенно велики. Они сформировались в мелком морском бассейне, занимавшем территории нынешних штатов Айдахо, Невада, Юта, Колорадо, Вайоминг и Монтана. Обогащенные фосфатом осадки (так называемая формация Фосфория), покрывают площадь более 160 тыс. км2 и достигают мощности 140 м. Однако мощность фосфатного пласта обычно равна 1 м и менее. Поэтому месторождения могут рассматриваться только в роли потенциального ресурса, общий тоннаж которого, однако же, огромен.
Небольшие по размеру нодули (конкреции) апатита обычны в некоторых известняках, сформировавшихся на дне неглубоких морей. Большие скопления нодулей, образовавшихся в результате непосредственного осаждения из воды, или при вторичном обогащении в виде слоев гравелитов, представляют собой ценные месторождения фосфоритов. Огромные фосфатные месторождения «наземной гальки» во Флориде являются источником 85 % современной фосфатной продукции США. Это вторичные концентрации фосфатных нодулей, первоначально находившихся в миоценовых известняках. Известная в штате Теннесси продуктивная площадь включает остаточные месторождения фосфоритов, образовавшихся при выветривании нодулесодержащих известняков.
Основные страны — продуценты фосфатов располагают и основными их запасами, которые действительно огромны. В 1982 г. они превышали 40 млрд. т. Однако пестрое географическое распределение известных ресурсов увеличивает транспортные расходы и тем самым общие издержки на производство удобрений. Поэтому такие страны, как Австралия, с большими площадями земель, нуждающихся в фосфорных удобрениях, продолжают поиски и разработку исследовательских программ в надежде открыть залежи, доступные для добычи. В результате найдено крупное месторождение в Квинсленде, однако высокая стоимость транспортировки сырья не позволяет пока начать его эксплуатацию.
Потенциальные ресурсы фосфора велики. Поиски же фосфатных месторождений были не настолько тщательными, чтобы уверенно ответить на вопрос, будут ли открыты новые крупные месторождения. Частично это объясняется экономическими трудностями, обусловленными конкуренцией вновь открытых месторождений с уже существующими рудниками. Успеху поисков препятствуют также трудности диагностики богатых фосфором пород. Даже для специалистов фосфатные породы часто неотличимы от простых сланцев или известняков. Следовательно, можно надеяться, что дополнительно будут открыты крупные месторождения фосфоритов.
Большой потенциальный ресурс фосфора ныне уже очевиден. На ряде континентальных шельфов обнаружены миоценовые корки и конкреции апатита, которые по способу образования близки формирующимся в настоящее время отложениям фосфатов. Эти образования по существу аналогичны богатым фосфорным месторождениям Флориды и Марокко, где они выведены на поверхность континента. К сожалению, качество этих морских отложений хуже по сравнению с их наземными аналогами, но тоннаж данного ресурса велик: возможно, он соизмерим с ныне зарегистрированными запасами. Следовательно, обеспеченность человечества фосфором, так же как азотом и калием, очень высока, и нет причин опасаться сокращения производства продуктов питания. Тем не менее на уровень применения удобрений могут повлиять такие факторы, как стоимость производства азотистых солей и стоимость добычи и перевозки фосфорного и калиевого сырья.
Сера. Сера имеет много областей применения и к элементам удобрений обычно не относится. Однако приблизительно 40 % мировой продукции используются для производства таких важных удобрений, как суперфосфат и сульфат аммония. Второй крупнейший потребитель серы — химическая промышленность; на ее долю приходятся 20 % всей продукции, из которых большая часть идет на производство инсектицидов и фунгицидов для борьбы с болезнями растений.
Поскольку сера является широкораспространенным элементом, ее источники различны и встречаются повсеместно. Например, море содержит огромные ресурсы сульфатов, а гигантские эвапоритовые месторождения, рассмотренные ранее, — громадные ресурсы CaSO4. Однако, как и в случае с ресурсами других элементов, целью поисков являются запасы серы, освоение которых требует наименьших затрат, при этом источники сырья могут быть различными в зависимости от местных условий. В 1982 г. 32 % мировой продукции приходились на элементарную или самородную серу.
Известны два главных источника самородной серы. Один из них, имеющий практическое значение главным образом в Японии, важность которого быстро снижается, — это серные вулканические газы, конденсирующие серу в близповерхностных жилах и пропитывающие <ею горные породы. Другой источник, в количественном отношении гораздо больший, — процесс вторичного обогащения за счет CaSO4. Определенные анаэробные бактерии извлекают кислород из твердых соединений, таких, как CaSO4, а энергию для этого получают в результате разложения органического вещества. В этом процессе участвует серия реакций, в ходе которых бактерии превращают органические соединения и CaSO4 в СаСО3 и S.
Этот процесс осуществляется там, где нефть служит источником энергии для жизнедеятельности бактерий. В США, Мексике и в ряде других мест бактериальное восстановление происходит в верхней части соляных куполов и в некоторых слоях эвапоритов. Когда соль поднимается из глубоко залегающих морских эвапоритов, ассоциирующийся с ней CaSO4 переносится в близповерхностную обстановку, где сера высвобождается в процессе бактериального восстановления. Из нескольких сотен известных в мире соляных куполов лишь немногие содержат промышленные концентрации самородной серы. Такие купола встречаются преимущественно вдоль побережья Мексиканского залива — от штата Алабама до Мексики. Они располагают большими запасами серы и в 1982 г. обеспечили 12 % ее мирового производства. Второй источник значительно больше, но свое признание он получил позднее, и его доля в общем производстве современной продукции пока невелика. Если циркулирующие приповерхностные воды локально выщелачивают NaCl и CaSO4 из эвапоритового слоя, нефть и бактерии могут заполнить образовавшиеся пустоты и восстановить сульфат до серы. В больших масштабах это происходит в западной части штата Техас, где только в Калберстон-Филд было обнаружено более 50∙106 т извлекаемой серы. Аналогичные месторождения известны в Ираке, Польше и СССР.
По сравнению с потреблением запасы серы невелики. Благодаря широким поискам за последние 30 лет во многих странах были открыты три альтернативных источника серы. Первый — H2S, или кислый газ, со держащийся в природном газе. Выпускавшийся ранее в атмосферу H2S теперь извлекается и окисляется до серы. Вторым источником, серы являются сульфидные руды редких металлов и колчеданные месторождения, в которых всегда присутствуют два сульфида железа пирит (FeS2) и пирротин FeS; из них сера извлекается как побочный продукт. Третьим источником является CaSO4, используемый в ряде европейских стран как новый материал для производства серной кислоты.
В 1982 г. мировое производство серы из всех источников достигло 52 млн. т, из них 10 млн. т было произведено в США. Запасы богатых руд самородной серы невелики, но ресурсы сульфидных и сульфатных руд огромны. Если успехи в развитии технологии обеспечат низкие цены на серу, получаемую. из альтернативных источников, у человечества не возникнет проблем с этим видом сырья. Сошлемся, в частности, на такой пример: снижение содержания двуокиси серы в дымах и атмосферных выбросах тепловых электростанций, работающих на угле, было достигнуто благодаря разработке новых способов извлечения двуокиси серы.
Химическое сырье
Неметаллические полезные ископаемые, используемые главным образом в качестве сырья для. химической промышленности, весьма разнообразны и имеют большое экономическое значение. Они обычно не являются главными полезными компонентами, но при использовании большинства из них руководствуются количеством, легкостью извлечения и, следовательно, низкими затратами. Для многих из них имеются заменители.
Наиболее важным членом этой группы является галит NaCl. Огромные ресурсы соли содержатся не только в морской воде, но и в морских эвапоритах. Поэтому проблема ресурсов переходит в проблему их добычи и перевозки. Например, в бассейне эвапоритов пермского возраста на юге и в центре США насчитывается более 150 тыс. км2 галитовых пластов суммарной мощностью 60 м, но сегодняшняя стоимость разработки этих месторождений высока, потому что они залегают сравнительно глубоко и удалены от основных рынков. Их добыча ведется, только на небольшом участке в штате Канзас.
Многие залежи недоступны для разработки, однако у природы есть интересный механизм переноса соли ближе к поверхности. Плотность галита — 2,2 г/см3, в то время как ассоциирующиеся с ним осадочные породы имеют плотность по меньшей мере 2,5 г/см3. Так как пласты соли легче и обладают способностью к пластическому течению, подобно льду в глетчере, они стремятся вверх и «протекают» сквозь перекрывающие их горные породы. Если последние достаточно слабы и, следовательно, могут быть прорваны поднимающейся солью, то длинные тонкие колонны, или стержни, всплывают из глубоко захороненных горизонтов осадочной соли. Известны случаи, когда столбы диаметром от 100 м до 2 км и более прорывались через перекрывающие их осадки мощностью не менее 12 км.
Соляные купола известны во многих регионах мира — в Европе, Южной Америке, СССР и на Среднем Востоке — но особенно часто они встречаются на побережье Мексиканского залива, где их число достигает нескольких сотен. Эти купола поднялись из эвапоритовых толщ, залегающих на 12 тыс. м ниже сегодняшней плоской равнины штатов Луизиана и Техас. Несколько из них разрабатываются на соль. Соль — существенный ингредиент питания, и 99 стран регулярно производят ее. Потребление соли в пищу составляет лишь малую долю из общего потребления, большая часть которого приходится на химическую индустрию — производство хлора и содового порошка Na2CO3 и коммунальные нужды — очищение мостовых и тротуаров от снега и льда. Неудивительно, что главные индустриальные державы — США, СССР и ФРГ — вместе с Китаем, родиной 20 % населения мира, потребляли в 1982 г. 50 % соли общей массой 182 млн. т.
Из всего комплекса. химического сырья, исключая петрохимическую продукцию, получаемую из горючих ископаемых, соль производится в наибольших масштабах. Среди других видов важное значение имеют: Na2CO3, используемый в, производстве бумаги, мыла, моющих средств и для обработки воды; Na2SO4, используемый для получения картона, моющих средств и добавок в дубящие и красящие вещества; бораты, такие, как бура Na2B4O7∙10H2O, используемые в производстве стекла (в качестве флюса), мыла, моющих средств, соединений для выделки шкур и антисептиков. Все эти минералы образуются путем осаждения из озерной воды в неморских эвапоритовых отложениях, и хотя отдельные месторождения не очень велики, распространены они достаточно широко.
Другие виды минерального сырья
Общий их список очень длинен, но только одна группа — абразивные материалы — технологически столь важна, что требует особого обсуждения.
Абразивы исключительно важны для обработки современных твердых сплавов и таких соединений, как карбид вольфрама. Алмаз, самый твердый из всех природных веществ, представляет собой наиболее важный ресурс. Эта плотная природная форма углерода требует для своего образования высоких давлений, которые достигаются только на глубинах 150 км и более. Образование материнских алмазоносных парод, называемых кимберлитами, связано с этими большими глубинами и с мантией; сами же по себе они редки. Кимберлиты выполняют узкие трубки взрыва, диаметр которых часто не превышает 50 м. Причины формирования и размещение кимберлитовых трубок остаются еще загадкой.
Кимберлиты являются коренными источниками алмазов, но не все они их содержат. На сегодня в Африке известны многие сотни кимберлитовых трубок, из которых менее 40 алмазоносны, но и из них треть не слишком богаты, чтобы оправдать разработку. На других континентах процент даже ниже, и за пределами Африки только в Якутии (СССР) и в северо-западной Австралии открыты кимберлиты, разработка которых может быть рентабельной. Даже в богатейших кимберлитах содержание алмазов очень низкое — не более чем 0,0000073 % (Это эквивалентно 0,2 г, или 1 кар, на каждые 3 т кимберлитов. — Прим. перев.). Кимберлиты и алмазы обнаружены на всех континентах, однако возможны открытия и новых богатых трубок. Например, алмазоносная трубка АК1 в северо-западной Австралии является, по-видимому, крупнейшей из найденных до сих пор, хотя открыта она была только в 1970-х годах. В Соединенных Штатах было обнаружено некоторое количество алмазов, однако большая их часть найдена в виде небольших россыпных месторождений. Алмазоносные кимберлиты в штате Арканзас являются, скорее, минералогическим курьезом, нежели потенциальными ресурсами. За 1970-е годы было открыто также несколько небольших алмазоносных кимберлитовых трубок в южной части штата Вайоминг и в северной части штата Колорадо. К сожалению, алмазы слишком малы по размерам и к тому же плохого качества, что не оправдывает их разработку.
Так как алмазы являются тяжелыми и весьма устойчивыми к разрушению минералами, они накапливаются в россыпях; более 90 % массы всех когда-либо извлеченных алмазов было получено из россыпей. Мы невольно вспоминаем о ювелирных изделиях, когда думаем об алмазах, но только 20 % добываемых алмазов может быть огранено, при этом бриллианты обеспечивают до 65 % всей стоимости алмазного производства. Остальные 80 % используются для промышленных целей, таких, как резание, штамповка, производство абразивов.
Со времени своего открытия в 1870 г. африканские месторождения были крупнейшими в мире поставщиками алмазов. Источником первой африканской продукции (из ЮАР) была кимберлитовая трубка, богатая ювелирными камнями, однако в последующие годы были открыты месторождения трубок в Танзании, Лесото, Ботсване и освоена добыча россыпей в Заире и Намибии. Африканские месторождения дали свыше 80 % мирового производства алмазов. Добыча алмазов в северной Сибири обеспечивает растущие потребности СССР в этом виде сырья. В течение последних 25 лет здесь было открыто более 400 кимберлитовых трубок на площади примерно 400X500 км2, расположенной к юго-западу от реки Лены. Возможно, трубок будет открыто много больше.
Измеренные запасы и возможные ресурсы драгоценных и технических алмазов велики, но дать их полную картину почти невозможно. Что касается технических алмазов, то технологический прогресс, в конце концов, указал путь самообеспечения. В 1955 г. компания «Дженерал Электрик» объявила об успешном синтезе технических алмазов, для чего используются специальные камеры для реакций при сверхвысоких давлениях. К 1981 г. промышленное производство алмазов только в США возросло до 11 400 кг в год; большое их производство приходится также на Швецию, ЮАР, Ирландию, Японию и СССР.
