Исследования, предпринятые с целью изучения функций пластид, оказались исключительно плодотворными в последние два-три десятилетия благодаря совершенствованию техники биохимического анализа и разработке надежных методов выделения неповрежденных хлоропластов, сохраняющих свою физиологическую активность вне клетки. Новые экспериментальные данные показали, что хлоропласта являются именно теми субклеточными структурами, в которых локализуется весь фотосинтетический аппарат. Таким образом, было окончательно опровергнуто господствовавшее долгое время представление о том, что фотосинтез невозможен вне целостной клетки, так как считалось, что в этом процессе принимают непосредственное участие не только пластиды, но и другие клеточные органоиды.
Реакция Хилла
Большую роль в изучении функции пластид сыграли работы Р. Хилла, послужившие своего рода толчком для новой серии широких исследований с целью воспроизведения реакций фотосинтеза на изолированных хлоропластах. Еще в 1937 г. Р. Хиллу удалось продемонстрировать способность изолированных зеленых пластид выделять молекулярный кислород на свету. Тем самым была доказана локализация этой световой реакции фотосинтеза в хлоропластах. Добавляя к суспензии хлоропластов в качестве окислителя соль трехвалентного железа, Р. Хилл установил, что под влиянием света такая смесь выделяет кислород и одновременно с этим происходит восстановление трехвалентного железа благодаря присоединению к нему электрона (e—) до двухвалентной формы:
Fe+++ + е— → Fe++
Вскоре выяснилось, что в этой реакции, получившей название реакции Хилла, помимо соли трехвалентного железа, акцепторами электронов, т. е. веществами, присоединяющими электроны, могут служить и некоторые другие окислители (например, хиноны). Но сущность превращений, происходящих в хлоропластах на свету и заканчивающихся выделением кислорода, оставалась некоторое время неясной. Прежде всего не была еще известна химическая природа донора — вещества, отдающего электрон или атом водорода, без чего невозможно восстановление трехвалентного железа или какого-либо другого акцептора. Только после того, как было доказано, что источником кислорода, выделяющегося при фотосинтезе, служит вода, стало возможным записать реакцию Хилла в общем виде следующим уравнением:
2А + 2Н2O [свет, хлоропласт]→ Н2А + O2,
где буквой «А» обозначен акцептор электрона или атома водорода. Из данного уравнения видно, что эта реакция приводит к окислению воды с выделением кислорода и восстановлению акцептора.
Важным достижением в познании механизма фотосинтеза явилось установление химической природы источника выделения кислорода. Правильно решить этот вопрос было весьма непросто, ибо таким источником может служить либо углекислый газ, либо вода, как это видно из суммарного уравнения фотосинтеза:
6СО2 + 6Н2O [свет, хлоропласт]→ С6Н12О6 + 6O2
ΔF = + 2,87 ∙ 106 дж (или + 686 ккал)
Образование одного моля гексозы при фотосинтезе сопровождается увеличением свободной энергии (ΔF) на 2,87 ∙ 106 дж (686 ккал) за счет поглощенной световой энергии.
В 1941 г. одновременно и независимо друг от друга в СССР акад. А. П. Виноградов и Р. В. Тейс и в США проф. С. Рубен и М. Камен установили, что кислород выделяется при фотосинтезе из воды, а не из СО2, как ошибочно считалось ранее. Доказательством этого в опытах А. П. Виноградова и Р. В. Тейс послужило обнаруженное ими совпадение изотопного состава кислорода, входящего в молекулу воды, и кислорода, выделяемого зеленым листом на свету. В обоих случаях отношение количества изотопов кислорода с атомным весом 18 и 16 (О18:О16) оказалось одним и тем же.
В природе, как известно, существуют три изотопа кислорода: О16, О17 и О18, причем соотношение между ними неодинаково у кислорода разного происхождения. В частности, для кислорода воды характерно наименьшее количество О18, тогда как содержание этого изотопа в кислороде углекислого газа, наоборот, наибольшее. Анализируя изотопный состав кислорода, обычно определяют отношение О18 к О16; содержание же О17 настолько низкое, что его не учитывают.
С. Рубен пошел по несколько иному пути, использовав для опытов с одноклеточной зеленой водорослью хлореллой искусственно синтезированную углекислоту или воду с различным содержанием изотопа О18. Изменения изотопного состава образующегося при фотосинтезе кислорода имели место только в тех случаях, когда для опытов бралась искусственно синтезированная вода, а не CO2. К тому же эти изменения совпадали с количественным отношением О18 к О16 в молекуле искусственно синтезированной воды, в которой суспензировались клетки хлореллы.
Фотосинтетическое фосфорилирование. Физиологическая активность изолированных хлоропластов, как показывают современные данные, не ограничивается способностью к реакции Хилла. Сравнительно недавно установлено и другое чрезвычайно важное свойство изолированных хлоропластов — способность осуществлять фотосинтетическое фосфорилирование. В результате этого процесса синтезируется аденозинтрифосфат (АТФ) путем присоединения неорганического фосфата к аденозиндифосфату (АДФ), или, другими словами, путем фосфорилирования АДФ. По современным представлениям, фотофосфорилированию принадлежит решающая роль в превращении растениями при фотосинтезе энергии квантов света в химическую энергию. Выше отмечалось, что энергия кванта света, поглощенного молекулой хлорофилла, передается электрону, который переходит в результате этого на более высокий энергетический уровень, т. е. возбуждается. При синтезе АТФ энергия возбуждения электронов трансформируется в химическую энергию его фосфатных связей.
В 1954 г. обнаружено два типа фотофосфорилирования: циклическое фосфорилирование и нециклическое.
Циклическое фотофосфорилирование протекает согласно такому уравнению:
АДФ + Н3РO4 [свет]→ АТФ + Н2O
Структурная формула АТФ показывает, что его молекула состоит из остатка азотистого основания аденина, соединенного с остатком углевода рибозы и с тремя остатками фосфорной кислоты. Один из остатков фосфорной кислоты соединен с пятым углеродным атомом рибозы простой эфирной связью, запас энергии которой невелик, примерно 8,37—12,56∙103 дж (2—3 ккал) на 1 моль. Два других остатка образуют богатые энергией связи, которые поэтому называются макроэргическими и обозначаются не черточкой, как обычно, а знаком Запас энергии в такой связи составляет в среднем 33,49 — 41,87 ∙ 103 дж (8—10 ккал) на 1 моль. Это означает, что при отщеплении от АТФ одной грамм-молекулы фосфорной кислоты в результате гидролиза макроэргических связей выделяется 33,49 — 41,87 ∙ 103дж (8—10ккал).
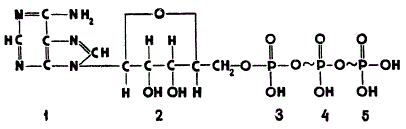
Строение аденозинтрифосфорной кислоты (АТФ): 1 — остаток аденина; 2 — остаток рибозы; 3, 4, 5 — остатки фосфорной кислоты
Благодаря наличию в АТФ макроэргических связей это соединение справедливо считается аккумулятором солнечной энергии, накопленной растением в удобной для использования форме. При «разрядке» такого своеобразного аккумулятора, т. е. при гидролизе АТФ, высвобождаются большие количества энергии, которая используется на различные ферментативные реакции, идущие с затратой энергии. Образование АТФ при фотофосфорилировании может рассматриваться как «зарядка» такого аккумулятора.
При нециклическом фосфорилировании, помимо синтеза АТФ, происходит восстановление никотинамидадениндинуклеотидфосфата (НАДФ, трифосфопиридиннуклеотид (ТПН) по старой терминологии) и выделение молекулярного кислорода:
2НАДФ + 2Н2O + 2АДФ + 2Н3РO4 [свет]→ 2НАДФ ∙ Н2 + 2АТФ + O2
Если при циклическом фосфорилировании вся биохимически эффективная энергия квантов света используется для образования АТФ, то здесь только часть этой энергии запасается в виде макроэргических связей АТФ, а часть расходуется на восстановление НАДФ и на выделение кислорода.
Считается, что восстановление СО2 до уровня углеводов непосредственно не зависит от действия света и может осуществляться в темноте. Энергию для этих реакций поставляет АТФ — этот универсальный источник энергии, а роль восстановителя выполняет НАДФ ∙ Н2.
НАДФ ∙ Н2 представляет собой динуклеотид, т. е. имеет в своем составе два нуклеотида. Каждый нуклеотид состоит из остатков трех различных типов веществ: азотистого основания, углевода рибозы и фосфорной кислоты. Азотистым основанием в одном из нуклеотидов служит пиридиновое производное амидникотиновой кислоты, а во втором — аденин, относящийся к пуриновым основаниям. Вместо рибозы второй нуклеотид содержит ее фосфорный эфир — рибозофосфат. В молекуле НАДФ нуклеотиды соединяются друг с другом своими остатками фосфорной кислоты.
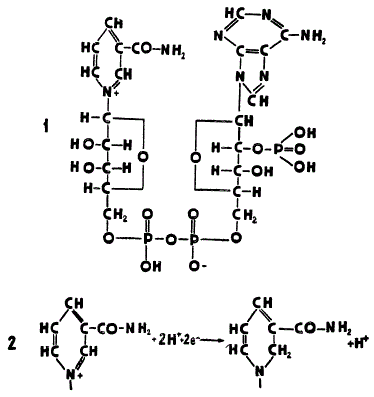
Строение и восстановление никотинамид-адениндинуклеотидфосфата: 1 — строение НАДФ (окисленная форма); 2 — восстановление остатка никотинамида
Активной группой НАДФ, способной восстанавливаться и повторно окисляться, является кольцо никотинамида. От окисляемого вещества (донора) отнимается два иона водорода и два электрона. Один из этих электронов соединяется при восстановлении НАДФ с положительно заряженным атомом азота, а другой электрон и ион водорода, вместе составляющие атом водорода, присоединяются к рядом расположенному атому углерода. Второй ион водорода соединяется не с остатком никотинамида, а с отрицательно заряженным кислородом одного из остатков фосфорной кислоты в молекуле НАДФ. Восстановленную форму сокращенно обозначают НАДФ ∙ Н2.
О двух пигментных системах
В настоящее время коренным образом пересматривается имевшая широкое распространение концепция о том, что в основе фотосинтеза лежит единая фотохимическая реакция. Большинством ученый сейчас принимается новая схема фотосинтеза, включающая не одну, а две фотохимические реакции, которые осуществляются с помощью двух различных пигментных систем.
Обоснованием наличия двух фотохимических реакций послужил эффект Эмерсона, установленный в ходе изучения эффективности фотосинтеза при освещении растений светом разной длины волны. Результаты этих опытов, графически изображенные на рисунке, показывают, что свет разной длины волны неравнозначен по своей эффективности для процесса фотосинтеза.
Эффективность превращения световой энергии в химическую энергию органических веществ можно характеризовать величинами квантового расхода или квантового выхода фотосинтеза. Квантовый расход показывает, сколько квантов света должно быть поглощено растением для выделения одной молекулы кислорода. Квантовый выход, напротив, характеризуется отношением числа поглощенных квантов света к числу молекул выделенного кислорода, т. е. это величина обратная квантовому расходу. Изучение квантового выхода фотосинтеза у различных видов растений показывает следующее.
Падение квантового выхода при 480∙10-9 м указывает на незначительную эффективность использования для фотосинтеза лучей этой области спектра, которые сильно поглощаются каротиноидами, а не зелеными пигментами. Наибольшая и почти постоянная эффективность наблюдается в области между 580 и 680 ∙ 10-9 м, (5800—6800 Å). Зато в далекой красной части спектра при длинах волн, превышающих 685 ∙ 10-9 м, начинается очень резкое падение квантового выхода, и при 700 ∙ 10-9 м фотосинтез почти полностью прекращается. Такое резкое падение эффективности фотосинтеза казалось совершенно невероятным и в течение ряда лет оставалось необъяснимым, так как в этой длинноволновой красной области спектра обнаруживается еще хорошее поглощение света хлорофиллом a, находящимся в живых клетках.
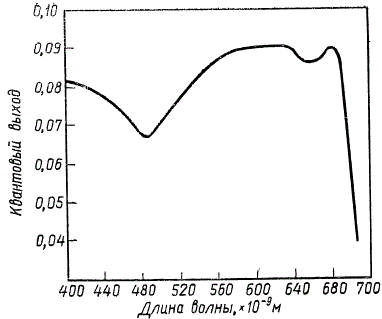
Зависимость квантового выхода фотосинтеза от длины волны падающего света у хлореллы (по Р. Эмерсону с соавторами)
Дальнейшие исследования привели к открытию так называемого эффекта усиления Эмерсона. Добавление к далекому красному свету (700∙10-9 м) более коротковолнового света (650 ∙ 10-9 м) вызывает значительное увеличение интенсивности фотосинтеза. Причем скорость выделения кислорода в случае добавления коротковолнового света оказывается большей, чем сумма скоростей, получаемых при освещении растений либо далеким красным, либо более коротковолновым светом в отдельности. Низкая эффективность далекого красного света объясняется тем, что при его поглощении возбуждается только одна пигментная система, ее называют первой пигментной системой и сокращенно обозначают ПСI. Добавление более коротковолнового света возбуждает вторую пигментную систему (ПСП), и в этом случае далекий красный свет используется с гораздо большей эффективностью, что и наблюдается при эффекте усиления. Высокая интенсивность фотосинтеза обеспечивается в данном случае строго сбалансированным возбуждением обеих пигментных систем. Если же одна из систем поглощает недостаточно света соответствующей длины волны, согласованность их совместной работы нарушается и происходит резкое падение интенсивности фотосинтеза.
Наряду с эффектом Эмерсона недавно были получены и другие экспериментальные данные, подтверждающие участие двух пигментных систем в фотохимических реакциях. Одним из важных достижений в этом отношении является осуществление механического разделения пигментных систем. С помощью обработки ультразвуком, поверхностно активными веществами с последующим дифференциальным центрифугированием и других методов удается получать легкие фрагменты хлоропластов, обогащенные фракцией первой пигментной системы, и более тяжелые фрагменты, обогащенные фракцией второй пигментной системы.
Первая пигментная система универсальна, т. е. присуща всем фотосинтезирующим организмам. Бактерии имеют только одну пигментную систему, которая, по-видимому, соответствует первой пигментной системе высших растений и водорослей.
Выше отмечалось, что бактерии способны только к бактериальному фотосинтезу (фоторедукции) без выделения молекулярного кислорода. На основании того, что эффект Эмерсона не обнаруживается у бактерий, сделан вывод об отсутствии у них второй пигментной системы, участвующей у высших растений и водорослей в окислении воды с выделением кислорода.
У зеленых растений первая пигментная система включает длинноволновые формы хлорофилла a с максимумом поглощения при 683 ∙ 10-9 м (6830 Å) и больше. Одна из форм хлорофилла a с максимумом поглощения при 700∙10-9 м была описана американским ученым Б. Коком как особо важная и обозначена П700. Иногда эта форма обозначается еще как хлорофилл a1. Кроме того, в первую систему входит небольшое количество хлорофилла b.
Ко второй пигментной системе относятся формы хлорофилла a с максимумом поглощения около 670 и 680∙10-9 м, а также вспомогательные пигменты и большая часть хлорофилла b с максимумом поглощения при 650∙10-9 м. У бурых, красных и сине-зеленых водорослей вторая пигментная система содержит коротковолновые формы хлорофилла a и основное количество вспомогательных пигментов, а в первую входят длинноволновые формы хлорофилла a и незначительные количества вспомогательных пигментов.
Большое значение для процесса фотосинтеза имеет явление миграции энергии поглощенных квантов света от одних молекул пигмента к другим и «стекание» этой энергии к активным центрам фотохимических систем, в которых и осуществляются фотохимические превращения. Хотя механизм миграции энергии возбуждения окончательно еще не выяснен, имеется основание считать, что в течение чрезвычайно короткого промежутка времени, порядка 5∙10-9 сек, поглощенный квант света успевает пройти через несколько сотен молекул пигмента. Квант продолжает мигрировать до тех пор, пока он не излучится при флуоресценции, не растратится в тепло либо не будет использован в фотохимической реакции. Было установлено, что каротиноиды могут передавать хлорофиллу a до 40—50%, а фукоксантин — даже до 70% поглощенной ими световой энергии. Такие вспомогательные пигменты, как фикоэритрин, фикоциан и хлорофилл b, передают хлорофиллу a еще больше энергии, от 80 до 96%.
О миграции энергии убедительно свидетельствует тот факт, что основным флуоресцирующим веществом у растений служит хлорофилл a даже в тех случаях, когда свет поглощается другими пигментами. Так, например, при освещении раствора пигментов светом такой длины волны, который возбуждает главным образом хлорофилл b наблюдается не его флуоресценция, а флуоресценция хлорофилла a. Следовательно, хлорофилл a получает энергию для своего возбуждения от хлорофилла b. Однако такой переход кванта сопровождается частичным рассеиванием его энергии. Это объясняется тем, что максимум поглощения хлорофилла a приходится на более длинноволновую область спектра, т. е. для перехода его молекулы в возбужденное состояние достаточен квант света с меньшим, чем для возбуждения молекулы хлорофилла b, запасом энергии. Отсюда понятно, что переход кванта в обратном направлении — к хлорофиллу b невозможен без притока дополнительной энергии.
Как правило, перенос энергии происходит лишь в одном направлении: от молекул пигмента, имеющего максимум поглощения в более коротковолновой области спектра, к молекулам другого пигмента с более длинноволновым максимумом. Поэтому в смеси фотосинтетических пигментов, присутствующих в пластиде, поглощенная каротиноидами энергия переносится сначала к хлорофиллу b, а от него к хлорофиллу a. У водорослей, имеющих еще и другие дополнительные пигменты, поглощенная энергия мигрирует от каротиноидов сначала к фикоэритрину, фикоциану, затем к хлорофиллам с или b и, наконец, к хлорофиллу a. Таким образом, хлорофилл a, представляя собой основной, главный компонент и первой, и второй пигментной системы, способен собирать энергию квантов, поглощенных другими пигментами. В дальнейшем эта энергия передается улавливающим центрам, которые осуществляют фотохимические реакции. Причем необходимо подчеркнуть, что для улавливания «блуждающих» по системе квантов не обязательно присутствие больших количеств пигмента. Его содержание может быть незначительным, не обеспечивающим заметного прямого поглощения света, но оно может быть вполне достаточным для того, чтобы служить своеобразной «ловушкой» квантов, первоначально поглощенных другими пигментами. Так, количество П700 весьма невелико, одна его молекула приходится на 300—500 молекул хлорофилла a1 тем не менее именно этот пигмент служит эффективной «ловушкой» фотонов в первой пигментной системе. Из всех фотосинтетических пигментов П700 имеет самый длинноволновый максимум поглощения, т. е. его возбужденное состояние соответствует наиболее низкому энергетическому уровню. Мигрирующий в первой пигментной системе квант может легко влететь в молекулу П700, теряя при этом часть своей энергии, но выйти из такой «ловушки» и продолжать дальше блуждать он не может, так как обладает уже недостаточным для этого запасом энергии.
Таким образом, молекула П700 получает кванты от окружающих ее многочисленных молекул хлорофилла a, выполняя тем самым чрезвычайно важную роль активного центра. Вся энергия системы в конечном счете стекается к таким центрам, прежде чем она будет использована в процессе фотосинтеза. Ниже мы покажем, что молекулы П700 не только поставляют энергию для фотохимических превращений, но и сами принимают в них непосредственное участие.
Во второй пигментной системе также, вероятно, существуют свои улавливающие энергию центры, аналогичные П700. Некоторые ученые считают, что роль «ловушек» квантов во второй пигментной системе выполняет одна из форм хлорофилла a, имеющая максимум поглощения при 680∙10-9 м и получившая поэтому условное обозначение П680, или aii. Однако такая точка зрения не является общепризнанной и требует дальнейшего экспериментального обоснования.
Световая фаза фотосинтеза
Всю совокупность фотосинтетических реакций принято подразделять на две фазы — световую и темновую. Для световой фазы характерно то, что энергия солнечной радиации, поглощенная пигментными системами, трансформируется в химическую энергию связей АТФ и НАДФ ∙ Н2. Темновая фаза осуществляется без непосредственного поглощения света. Цепь реакций, приводящих к восстановлению СО2 до уровня органических веществ на этой фазе, идет за счет использования АТФ и НАДФ ∙ Н2.
Чтобы лучше понять сущность фотохимических реакций и процессов, которые происходят на световой фазе у высших растений и водорослей, воспользуемся одной из схем, предложенных в последнее время.
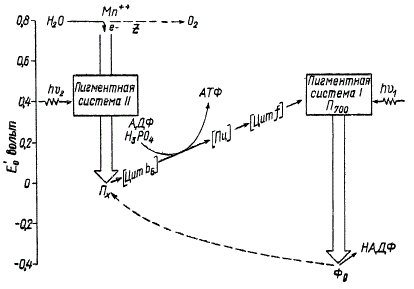
Схема световой фазы фотосинтеза (по Л. Вернону). Стрелки указывают направление движения электрона
Процесс фотосинтеза представляет собой цепь окислительно-восстановительных реакций, заканчивающихся в конечном итоге окислением воды и восстановлением углекислого газа. Суть любой окислительно-восстановительной реакции, как известно, сводится к переносу атома водорода от молекулы-донора (восстановитель) на молекулу-акцептор (окислитель). В результате этого донор окисляется, а акцептор восстанавливается. Первичным донором в процессе фотосинтеза является вода, а конечным акцептором — углекислота.
Часто вместо переноса атома водорода в окислительн-восстановительных реакциях происходит перемещение электрона от донора к акцептору. В дальнейшем для простоты изложения будет говориться только о переносе электронов, хотя на самом деле в цепи окислительно-восстановительных реакций фотосинтеза происходят и такие реакции, в ходе которых переносится атом водорода, а не электрон.
На рисунке показаны основные звенья цепи переноса электронов на световой фазе. Для того чтобы нагляднее представить энергетические изменения на протяжении электрон-транспортной цепи, схемы фотосинтеза приводят на фоне масштаба окислительно-восстановительных потенциалов (Е’0), выраженных в вольтах.
Окислительно-восстановительный потенциал — это величина, характеризующая разность между энергетическими уровнями окисленной и восстановленной форм вещества. Каждой окислительно-восстановительной паре свойственно определенное значение разности потенциалов. Например, при восстановлении кислорода до воды окислительно-восстановительный потенциал пары кислород-вода составляет около +0,8 в, а окислительно-восстановительный потенциал пары СО2 — углевод равен примерно —0,4 в (при pH 7). Чем выше значение окислительно-восстановительного потенциала, тем больше окисляющая способность пары; чем ниже его величина, тем больше восстанавливающая способность.
В настоящее время многие исследователи признают возможным поступление световой энергии в систему, осуществляющую процесс фотосинтеза, не в одном, а в двух местах электрон-транспортной цепи, в которых и происходят фотохимические реакции. Одна из таких реакций непосредственно связана с поглощением квантов света первой пигментной системой и переходом в возбужденное состояние ее активного центра — П700. Молекулы этого пигмента как бы вмонтированы в электрон-транспортную цепь и являются одним из важнейших ее звеньев. Они непосредственно участвуют в реакции восстановления ферредоксина, претерпевая при этом обратимые окислительно-восстановительные превращения. Возбужденная молекула П700 освобождает электрон с большим запасом энергии, часть которой была им получена в результате поглощения кванта света. Таким образом, первичный результат действия световой энергии состоит в изменении химических свойств молекулы П700, которая отдает электрон и переходит в окисленное состояние, приобретая способность снова присоединять электрон и повторять заново такой же цикл превращений.
Акцептором электронов от П700 служит ферредоксин (белок, содержащий железо), отличающийся высоким отрицательным окислительно-восстановительным потенциалом, который близок к потенциалу газообразного водорода, а именно — 0,42 в при pH 7. Восстановление ферредоксина протекает с поглощением энергии, так как электрон переходит от системы с большим окислительно-восстановительным потенциалом (+ 0,4 в) к системе с меньшей его величиной (— 0,42 в). Энергию, необходимую для этой реакции, поставляют кванты света, поглощенные первой пигментной системой. По мнению некоторых исследователей, роль непосредственного акцептора электронов от П700 выполняет не ферредоксин, а другое, пока точно не установленное вещество с еще большим отрицательным окислительно-восстановительным потенциалом (до —0,6 в), способное восстанавливать ферредоксин в темноте. Однако ферредоксин — это пока что единственное соединение с резко выраженной восстанавливающей способностью, которое выделено из хлоропластов в чистом виде и достаточно хорошо изучено.
Ферредоксин при участии особого фермента (ферредоксин — НАДФ — редуказа) восстанавливает НАДФ до НАДФ ∙ Н2. Эта реакция сопровождается потерей энергии и может протекать в темноте, поскольку окислительно-восстановительный потенциал у НАДФ ∙ Н2 равен — 0,32 б, а у ферредоксина он равен — 0,42 в. В дальнейшем, на темновой фазе фотосинтеза НАДФ ∙ Н2 принимает участие в восстановлении углекислого газа.
Но каким же образом происходит восстановление молекулы П700, отдавшей свой электрон ферредоксину? Как видно на схеме, окисленная молекула П700 возвращается в исходное состояние, восполняя потерю электрона за счет другой фотохимической реакции, которая осуществляется второй пигментной системой. Под действием поглощенной световой энергии активный центр второй пигментной системы возбуждается и передает электрон на акцептор, которым, по всей видимости, является пластохинон. В результате этого пластохинон восстанавливается фотохимически и приобретает окислительно-восстановительный потенциал, близкий к нулю.
Затем электрон от пластохинона передается через ряд темновых окислительно-восстановительных реакций на цитохром f с помощью комплекса промежуточных переносчиков электронов. Об этом комплексе известно пока еще мало. Имеются основания считать, что он включает в себя цитохром b6, пластоцианин (содержащий медь окрашенный белок) и, возможно, некоторые другие соединения.
Цитохромы — это белки, в состав которых входит железо. Они играют исключительно важную роль в окислительно-восстановительных реакциях, причем в их отсутствии процесс фотосинтеза не может осуществляться. Это объясняется тем, что цитохромы связывают друг с другом обе фотохимические системы, обеспечивая их взаимодействие. Электрон от возбужденной второй пигментной системы через пластохинон и комплекс промежуточных переносчиков передается на окисленный цитохром f. Восстанавливаясь, цитохром f становится донором электронов для П700. Таким образом, цитохром f и П700 окисляются за счет энергии, поглощенной первой пигментной системой, а восстанавливаются за счет энергии, поглощенной второй пигментной системой. Нарушение четкой согласованности и взаимосвязи двух фотохимических реакций, например при отсутствии цитохромов, приводит к тому, что молекулы П700 перестают получать электроны от второй пигментной системы и этим самым блокируется работа первой пигментной системы. Об этом же свидетельствуют следующие экспериментальные данные. При освещении растений одним только красным светом с длиной волны около 705 ∙ 10-9 м (7050 Å) цитохром f и П700 остаются в окисленной форме, так как вторая пигментная система не возбуждается при освещении таким светом и не поставляет электроны для их восстановления.
Как известно, окисление воды с выделением кислорода составляет специфическую черту, отличающую фотосинтез высших растений и водорослей от бактериального фотосинтеза (фоторедукции). Механизм процесса окисления воды до сих пор остается нерасшифрованным, и участок электрон-транспортной цепи вода — вторая пигментная система изучен, пожалуй, наиболее слабо. Известно только, что процесс окисления воды состоит из ряда последовательных реакций, приводящих к разрыву прочных молекул воды с отщеплением атомов водорода и выделением молекулярного кислорода. Доказана необходимость наличия ионов марганца и хлора для выделения кислорода при фотосинтезе, хотя сам механизм действия этих ионов еще неясен. На основании своих исследований Д. И. Сапожников с сотрудниками считают весьма вероятным участие в переносе кислорода при фотосинтезе некоторых из ксантофиллов, а именно системы лютеин — виолаксантин.
Окисление воды — важнейший процесс, поставляющий электроны для восстановления активного центра второй пигментной системы. Правда, химическая природа непосредственного донора электронов для второй пигментной системы пока не установлена, поэтому на схеме он обозначается буквой z. От донора z электрон воды переносится к НАДФ путем двух последовательных фотохимических реакций.
Такова в общих чертах схема пути переноса электронов на световой фазе фотосинтеза. Следует, конечно, понимать, что в действительности электрон-транспортная цепь, по-видимому, намного сложнее, чем она выглядит на представленной здесь схеме.
На основании анализа схемы можно сделать чрезвычайно важный вывод о том, что растение запасает энергию в двух местах электрон-транспортной цепи, именно там, где благодаря фотохимическим реакциям электрон переходит от системы с большей величиной окислительно-восстановительного потенциала к системе с гораздо меньшей его величиной. Так, при фотохимическом восстановлении пластохинона электрон переходит от системы с окислительно-восстановительным потенциалом, равным +0,80 б, к системе с окислительно-восстановительным потенциалом, близким к нулю, а при фотохимическом восстановлении ферредоксина П700 обеспечивает транспортировку электронов от системы с Е’0, равным +0,4 в, к системе с равным —0,44 а. Переход электрона к системе с меньшим окислительно-восстановительным потенциалом означает повышение запаса его энергии и восстановительной способности за счет энергии квантов света, поглощенных пигментными системами. Следовательно, реакции восстановления пластохинона и ферредоксина не могут идти самопроизвольно, они сопровождаются поглощением солнечной радиации, в результате чего происходит запасание части энергии поглощенных квантов света в виде химической энергии системы, получившей электрон.
Весь путь электрона, начиная с окисления воды и кончая восстановлением НАДФ, обычно выделяют как фотохимическую, или световую, фазу фотосинтеза, обеспечивающую запасание растением энергии. На самом же деле, помимо фотохимических реакций, возбуждаемых энергией поглощенных квантов света, эта фаза фотосинтеза включает в себя и такие химические реакции, которые не нуждаются в непосредственном действии света. Условно их называют темновыми реакциями, хотя они могут протекать как в темноте, так и на свету. Наибольший интерес представляют темновые окислительно-восстановительные реакции, связывающие обе фотохимические системы. На участке пластохинон — П700 электрон переходит в соответствии со схемой от системы, имеющей Е’0 около нуля, к системе с равным примерно +0,4 в. Такой перенос электрона к системе с большим окислительно-восстановительным потенциалом, а следовательно, с меньшим запасом энергии, сопровождается выделением части энергии, используемой в сопряженно идущей реакции фосфорилирования на синтез АТФ.
Описанная выше электрон-транспортная цепь, начиная от окисления воды с выделением кислорода и кончая восстановлением НАДФ, фактически представляет собой путь, совершаемый электронами в процессе нециклического фосфорилирования. На схеме показано место двух фотохимических реакций в нециклическом транспорте электронов, а также отмечено место образования АТФ на участке между пластохиноном и цитохромом f. Некоторые исследователи считают, что и в других местах электрон-транспортной цепи не исключена возможность синтеза соединений с макроэргическими связями. При нециклическом фосфорилировании энергия возбуждения электронов превращается в химическую энергию макроэргических связей АТФ, а также расходуется на восстановление НАДФ и разложение воды с выделением кислорода.
Если же окисление НАДФ ∙ Н2 до НАДФ замедляется или даже прекращается вовсе, когда, например, тормозится процесс восстановления углекислого газа, возможно обратное транспортирование электрона к П700, а именно: электрон, полученный ферредоксином от П700, переходит на пластохинон, а от него через цитохромы возвращается к П700. Путь электрона от ферредоксина к пластохинону обозначен на схеме пунктиром. На участке пластохинон — цитохром f сопряженно происходит процесс фосфорилирования АДФ до АТФ. В связи с тем что электрон, пройдя замкнутый (циклический) путь, снова возвращается к молекуле П700, этот тип фосфорилирования получил название циклического. Поскольку циклическое фосфорилирование не сопровождается выделением кислорода и восстановлением НАДФ, энергия возбуждения электрона расходуется только на синтез АТФ. В зависимости от количества НАДФ в системе осуществляется либо нециклическое фосфорилирование с участием обеих пигментных систем, либо циклическое, при котором «работает» лишь первая пигментная система. Если НАДФ ∙ Н2 интенсивно окисляется до НАДФ, то электрон от ферредоксина направляется к НАДФ и происходит нециклическое фосфорилирование, в противном случае электрон от ферредоксина переходит на пластохинон и имеет место циклический транспорт электрона. Таким образом, можно считать, что НАДФ выполняет роль физиологического регулятора, определяющего тип процесса фосфорилирования.
Темновая фаза фотосинтеза
О том, как происходит превращение CO2 в сложные органические соединения на темновой фазе фотосинтеза, долгое время не знали практически ничего. Бурное развитие биохимии, широкое использование различных современных методов исследования— все это обеспечило в течение последних 20 лет огромные успехи в изучении проблемы фотосинтеза вообще и особенно в расшифровке пути образования органических веществ из углекислого газа. Реакции восстановления CO2 до уровня углеводов и некоторых других органических соединений происходят в растениях настолько быстро, что с помощью обычных методов химического анализа чрезвычайно трудно обнаружить промежуточные продукты и практически невозможно установить последовательность их превращений. Только использование радиоактивных изотопов, в первую очередь С14, в качестве метки, бумажной хроматографии, электрофореза и других методов позволило довольно легко обнаружить и выделить промежуточные продукты, а также отличить только что образовавшиеся вещества от веществ, аналогичных по химическому составу, но уже давно накопленных в клетке. Кроме того, посредством изменения времени, в течение которого растение находится в атмосфере с добавлением радиоактивной углекислоты, стало возможным по скорости включения С14 в те или иные промежуточные продукты определять последовательность их синтеза. С помощью С14O2 можно даже установить, в каком месте углеродной цепи происходит включение радиоактивной метки, что также позволяет судить о характере химических превращений и об их последовательности. Довольно детально были изучены и те ферментные системы, которые катализируют отдельные реакции взаимных превращений веществ в ходе восстановления СО2 до уровня углеводов.
Таким образом, на базе широких исследований, проведенных многочисленными лабораториями, удалось в основном проследить всю последовательность превращений простого соединения СО2 до уровня углеводов и некоторых других сложных органических веществ.
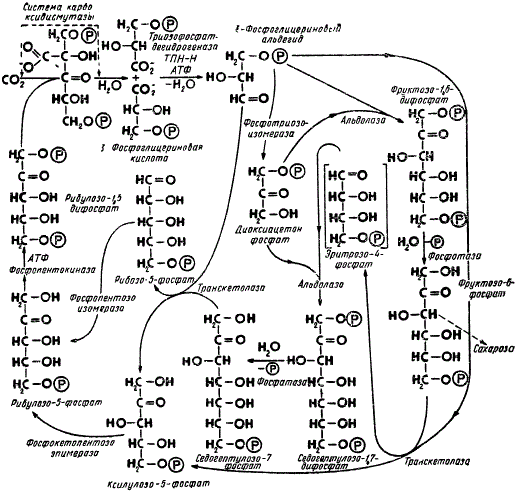
Схема фотосинтетического цикла восстановления углерода (по М. Кальвину): Р — условно обозначается остаток фосфорной кислоты — Н2РО3. Направление стрелок указывает последовательность превращения веществ
На рисунке представлена наиболее экспериментально обоснованная схема последовательности реакций восстановления СО2 до уровня углеводов, получившая название цикла Кальвина. Как видно из схемы, характерная особенность фотосинтетического восстановления углекислоты заключается в цикличности этого процесса. Соединение, первоначально присоединяющее СО2 (рибулозо-1,5-дифосфат), в результате целого ряда последовательных реакций регенерируется (возобновляется) до своего исходного состояния и становится способным присоединять новые молекулы СО2, а следовательно, повторять заново циклы таких же превращений.
Цикличность — очень важное свойство, обеспечивающее высокую производительность и саморегулируемость процесса восстановления СО2, а также многих других процессов, совершающихся в биологических системах.
К настоящему времени удалось уже выделить и изучить большинство промежуточных продуктов цикла Кальвина, а также многие ферменты, участвующие в различных превращениях углеводов. Все реакции этого цикла удалось воспроизвести изолированно в растворе. Согласно современным представлениям, на темновой фазе фотосинтеза восстанавливается карбоксильная группа (— СООН), образующаяся в результате присоединения CO2 к рибулозо-1,5-дифосфату под воздействием фермента карбоксидисмутазы.
Карбоксилирование рибулозо-1,5-дифосфата является по существу первой реакцией, вводящей CO2 в цикл Кальвина. Образующаяся при этом нестойкая шестиуглеродная кислота быстро распадается на две молекулы 3-фосфоглицерииовой кислоты, содержащей в своем составе три углеродных атома. Эта кислота подвергается восстановлению за счет НАДФ ∙ H2 при обязательном участии АТФ до 3-фосфоглицеринового альдегида, некоторая часть молекул которого превращается под влиянием фермента фосфотриозоизомеразы в свою изомерную форму — фосфодиоксиацетон. Затем эти изомеры (3-фосфоглицериновый альдегид и фосфодиоксиацетон) соединяются друг с другом при участии фермента альдолазы, образуя фруктозо-1,6-дифосфат. Это соединение в дальнейшем служит исходным материалом для синтеза сахарозы и различных полисахаридов, в том числе и крахмала. Таким образом, часть молекул 3-фосфоглицеринового альдегида расходуется в конечном счете на образование сахарозы и полисахаридов, которые выходят из цикла Кальвина и не принимают больше участия в его дальнейших превращениях.
В то же время другая часть молекул 3-фосфоглицеринового альдегида подвергается целому ряду сложных ферментативных превращений, заканчивающихся регенерацией рибулозо-1,5-дифосфата. При взаимодействии 3-фосфоглицеринового альдегида с фруктозо-6-фосфатом возникает цепь фосфорных эфиров углеводов, содержащих в своем составе по четыре, пять или семь атомов углерода. Большую роль в этих реакциях играют ферменты, катализирующие перенос целых атомных группировок от одних соединений к другим. Так, под действием транс-кетолазы концевая двууглеродная группа переносится от фруктозо-6-фосфата на 3-фосфоглицериновый альдегид с образованием ксилулозо-5-фосфата, а остаток молекулы фруктозо-6-фосфата превращается в эритрозо-4-фосфат. Этот же фермент участвует в переносе двууглеродной группы от седогептулозо-7-фосфата на 3-фосфоглицериновый альдегид, в результате чего возникают две пентозы: ксилулозо-5-фосфат и рибозо-5-фосфат. В дальнейшем при участии соответствующих ферментов эти пентозы переходят в изомерную форму, т. е. в рибулозо-5-фосфат, который затем подвергается фосфорилированию за счет АТФ. Таким образом, цикл восстановления CO2 завершается регенерацией рибулозо-1,5-дифосфата с более высокой реакционной способностью к карбоксилированию. Присоединением новой молекулы CO2 к рибулозо-1,5-дифосфату фотосинтетический цикл восстановления углерода начинается заново.
При фиксации одной молекулы CO2 образуются две молекулы 3-фосфоглицериновой кислоты, каждая из которых восстанавливается до 3-фосфоглицеринового альдегида с затратой молекулы НАДФ ∙ Н2 и молекулы АТФ. Превращение 3-фосфоглицериновой кислоты в 3-фосфоглицериновый альдегид — это по существу единственная восстановительная реакция цикла Кальвина. Еще одна молекула АТФ расходуется в другом месте цикла на фосфорилирование рибулозо-5-фосфата. Таким образом, всего на восстановление одной молекулы CO2 до уровня углеводов расходуется две молекулы НАДФ ∙ Н2 и три молекулы АТФ. Использование АТФ и НАДФ ∙ Н2 в цикле представляет собой тот механизм, посредством которого энергия квантов, накопленная на световой фазе фотосинтеза в виде химической энергии связей этих соединений, расходуется на темновой фазе в процессе синтеза органических веществ из CO2.
Еще сравнительно недавно многие ученые продолжали считать, что первыми и единственными продуктами фотосинтеза являются углеводы, а все остальные соединения образуются в результате их вторичных превращений. Однако исследованиями ученых (главным образом отечественных) была обоснована возможность возникновения при фотосинтезе и других веществ, таких, как органические кислоты, аминокислоты, вне связи со вторичными превращениями углеводов. Первое экспериментальное подтверждение возражения против представления об углеводах как первичных и единственных продуктах фотосинтеза было получено еще в 1894 г. В. В. Сапожниковым, а позже Ф. Н. Крашенинниковым (1901), К. А. Пуриевичем (1913), В. О. Таусоном (1946). В последнее время исследованиями А. А. Ничипоровича и других ученых было установлено, что в зависимости от вида растений, их физиологического состояния и условий выращивания (например, от условий азотного питания, освещения и т. п.) фотосинтетическое восстановление CO2 идет неодинаковыми путями и приводит к образованию органических веществ разного состава и качества.
С помощью радиоактивных изотопов и некоторых других современных методов было доказано, что из цикла Кальвина может выключаться не только фруктозо-6-фосфат, давая начало сахарозе и полисахаридам, но и другие промежуточные продукты. Причем отторжение из цикла продуктов неодинаковой химической природы обеспечивает широкие возможности для биосинтеза разнообразных органических веществ.
Последовательность включения радиоактивной метки в продукты фотосинтеза свидетельствует о том, что уже 3-фосфоглицериновая кислота способна отторгаться из цикла и служить исходным материалом для образования органических кислот и аминокислот. В результате непосредственного аминирования 3-фосфоглицериновая кислота превращается в аминокислоту серин (СН2—ОН—CH∙NH2—СООН). Кроме того, она может превращаться через фосфоенолпировиноградную кислоту в другую аминокислоту — аланин (СН3—СН∙NH2—СООН).
С другой стороны, фосфоенолпировиноградная кислота, присоединяя к себе углекислый газ и воду, дает начало четырехуглеродным органическим кислотам. Цепь реакций, приводящих к синтезу таких кислот, схематически представлена на рисунке.
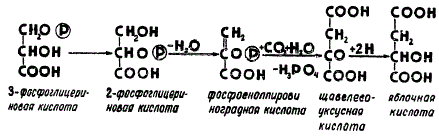
Схема реакций образования четырехуглеродных соединений из 3-фосфоглицериновой кислоты
Помимо фиксации CO2 посредством присоединения к рибулозо-1,5-дифосфату, в растениях может осуществляться карбоксилирование фосфоенолпировиноградной кислоты, а возможно, и некоторых других веществ. При карбоксилировании фосфоенолпировиноградной кислоты образуются не сахара, а органические кислоты — щавелевоуксусная и яблочная. Посредством присоединения аммиака с последующим восстановлением щавелевоуксусная кислота легко превращается в аспарагиновую кислоту (COOH—CH∙NH2—CH2—COOH).
По современным представлениям, при фотосинтетическом восстановлении CO2 в цикле Кальвина образуются не только углеводы, но и различные органические вещества, в том числе и азотистые соединения. Причем основное количество поглощенного пластидами углекислого газа, по крайней мере до 70—85%, включается в обмен веществ через цикл Кальвина благодаря карбоксилированию рибулозо-1,5-дифосфата и лишь незначительная часть фиксируется в результате присоединения CO2 к фосфоенолпировиноградной кислоте. Однако цикл Кальвина — это не единственный путь усвоения углекислоты растениями в процессе фотосинтеза.
Недавними исследованиями М. Хетча и К. Слэка показано, что в листьях сахарного тростника осуществляется иной путь фотосинтетического восстановления CO2, главной реакцией которого служит карбоксилирование фосфоенолпировиноградной кислоты, а не рибулозо-1,5-дифосфата. Он называется путем Хетча и Слэка.
Локализация световой и темновой фаз фотосинтеза в пределах хлоропласта
Большое число экспериментальных данных убедительно показывает, что все реакции световой фазы осуществляются в ламеллярных структурах — тилакоидах, тогда как восстановление CO2 на темновой фазе происходит в строме хлоропласта. Таким образом, световая и темновая фазы фотосинтеза в пределах хлоропласта оказываются разделенными не только во времени, но и в пространстве. Наиболее наглядным и убедительным доказательством справедливости такого представления могут служить, пожалуй, результаты опытов по изучению отдельных фракций пластид.
Световую и темновую фазы удалось физически разделить с помощью фракционирования содержимого хлоропластов на тилакоиды и строму. Для этого их сначала разрушают, например действием ультразвука, а затем центрифугируют при больших скоростях. В итоге такой обработки тилакоиды и их фрагменты оседают, а бесцветное вещество стромы остается в надосадочной жидкости. Изучение этих фракций показало, что реакцию Хилла и фотосинтетическое фосфорилирование (т. е. все процессы световой фазы, приводящие к окислению воды с выдедением молекулярного кислорода, восстановлению НАДФ и синтезу АТФ) осуществляют тилакоиды, а не строма.
Кроме того, экспериментально также было доказано, что реакции восстановления CO2 с образованием фосфорных эфиров сахаров локализованы в строме и что для их осуществления необходимо наличие НАДФ∙Н2 и АТФ. Когда к фракции стромы искусственно добавляли АТФ, НАДФ∙Н2 и С14O2, то вскоре наблюдали образование в темноте меченых по углероду органических веществ, аналогичных промежуточным продуктам цикла Кальвина при нормальном фотосинтезе.
О локализации световой и темновой фаз в пределах хлоропласта свидетельствуют и результаты химических анализов отдельных фракций как тилакоидов, так и стромы. Оказалось, что большинство известных соединений, участвующих в реакциях световой фазы, полностью сосредоточены в тилакоидах. Это прежде всего фотосинтетические пигменты, цитохромы f и b6, пластохинон, пластоцианин и, по-видимому, ферредоксин. В тилакоидах также присутствуют те ферменты, которые катализируют реакции световой фазы, тогда как строма содержит ферментные системы, принимающие участие в восстановлении CO2 на темновой фазе. Так, например, в строме хлоропластов обнаружено более 95% карбоксидисмутазы — фермента, катализирующего реакцию присоединения CO2 к рибулозо-1,5-дифосфату.
О многообразии функций хлоропластов
В настоящее время экспериментально установлено, что функции хлоропластов многообразны и далеко не ограничиваются ассимиляцией углекислого газа. Наряду с митохондриями «силовыми станциями» клетки, вырабатывающими универсальный источник энергии — АТФ, следует считать и хлоропласты. За счет энергии АТФ они способны восстанавливать не только CO2, но также (на свету) нитраты и сульфаты. Кроме того, в хлоропластах осуществляются синтетические процессы, приводящие к тому, что образуются полисахариды, липиды, пигменты, белки и некоторые другие вещества. В таких процессах принимают участие соответствующие ферментные системы, которыми эти органоиды клетки исключительно богаты. Такое многообразие функций указывает на чрезвычайно важное значение хлоропластов в обмене веществ клетки и в различных процессах ее жизнедеятельности.
Источник: Н.Н. Овчинников, Н.М. Шиханова. Фотосинтез. Пособие для учителей. Изд-во «Просвещение». Москва. 1972
