Раздел, занимающийся изучением действия гена, по предложению Р. Гольдшмидта в 1935 г. был назван физиологической генетикой.
Однако, изучение действия гена в системе онтогенеза правильнее относить к онтогенетике. Физиологическая генетика — более общее понятие. В раздел физиологической генетики можно включить изучение функционального состояния самого гена, исследование его изменчивости, его взаимосвязей в системе генотипа, а также анализ действия гена. Вся современная генетика по существу является физиологической. Физиологическая генетика изучает функциональные взаимосвязи всех систем клетки, обеспечивающих материальную непрерывность в ряду поколений. Исследование действия гена в определении признака или свойства, иными словами проблема ген — признак, является лишь одним из разделов физиологической генетики.
В цепи ген — признак протекают сложные процессы. Гены должны организовать работу всей клеточной системы. Но, видимо, гены не только обеспечивают прямую связь ядро — цитоплазма, но и обратную: цитоплазма — ядро. Гены определяют синтез определенных продуктов в определенное время и в определенной последовательности. Но эти же продукты в свою очередь могут оказывать влияние на функцию генов.
Когда и как начинает действовать ген? Этот вопрос является одним из основных в современной генетике.
Мы изложили современное представление о начальном механизме функционирования гена — механизме синтеза специфических белков по схеме ДНК — РНК — белок. Мы видели, что синтез белка осуществляется в рибосомах, что последовательность нуклеотидов в цепочке ДНК определяет последовательность аминокислот в полипептидной цепочке молекулы белка и что одно мутационное изменение приводит к изменению одной аминокислоты в белковой молекуле. Следовательно, первичное действие гена начинается с определения места включения аминокислоты при синтезе сложной белковой молекулы.
Однако одни только структурные гены, непосредственно отвечающие за синтез белка, не в состоянии обеспечить детерминацию развития. Исследование механизма действия и взаимодействия генов в процессе морфологической и функциональной дифференцировки остается главной задачей онтогенетики. Механизм действия гена является в настоящее время предметом исследования многих биологических дисциплин и ведется методами генетики, биохимии, иммуногенетики, цитогенетики, экспериментальной эмбриологии и многих других наук.
Мы уже касались генетических и биохимических методов изучения взаимодействия генов, определяющих образование пигментов. Из этих и других примеров, которые также были приведены, становится ясно, что изменение отдельных генов вызывает определенные изменения в химическом составе специфических веществ. Ген может контролировать как синтез определённых химических веществ, так и скорость различных реакций обмена веществ. Каким же образом химические изменения гена приводят к изменению обмена веществ и далее — к изменению фенотипа?
Удобным объектом для изучения действия мутантных генов, влияющих на биосинтез многих метаболитов, послужили микроорганизмы. С этой целью сначала были использованы различные биохимические мутанты нейроспоры.
Напомним, что нейроспора растет на питательной среде, содержащей минеральные соли, сахар и витамин В (биотин). В процессе роста формы дикого типа синтезируют все вещества, являющиеся необходимыми компонентами протоплазмы, — аминокислоты, витамины, нуклеиновые кислоты, полисахариды, липиды и другие вещества. Биохимические мутанты нейроспоры (ауксотрофы) вследствие действия мутантного гена теряют способность синтезировать какое-либо из указанных веществ и без добавки его в среду не растут. Было установлено, что потребность в одном определенном веществе у данного штамма связана с мутацией одного гена. Благодаря этому можно иметь штаммы с отдельными мутантными генами, блокирующими синтез определенных веществ. При этом следует иметь в виду, что в случае, если биосинтез какого-либо вещества представляет сложную цепь реакций, блокирование различных ступеней этой цепи в результате различных мутаций будет приводить к потребности в одном и том же конечном продукте или в том конкретном промежуточном метаболите, синтез которого блокирован.
Так, например, у нейроспоры были исследованы три мутанта, определяющие потребность в аргинине. Нормальный рост одного мутанта обеспечивается при условии добавки в среду аргинина, орнитина или цитруллина, второй мутант требует добавки в среду аргинина или цитруллина, а третий мутант — только аргинина. На основе этих данных устанавливается серия реакций биосинтеза аргинина. У указанных трех мутантов блокируются различные ступени в этой цепи биохимических реакций. В силу этого мутанты накапливают промежуточные продукты, образующиеся до блока, и поэтому способны расти лишь при добавке тех метаболитов, которые образуются после блока.
Другим примером изучения процессов биосинтеза в клетке может служить анализ синтеза триптофана и образования никотиновой кислоты также у нейроспоры. Последовательные этапы этого процесса были выявлены посредством выделения нескольких мутантов, не способных синтезировать никотиновую кислоту. Мутанты различались по потребности в определенном предшественнике никотиновой кислоты, без добавки которого они не росли на минимальной среде, и по накоплению того или иного метаболита. На этих мутантах было показано, что генетическое блокирование может возникать на любом из шести этапов, представленных на рисунке. Например, мутант, определяющий блок на стадии 4, накапливает триптофан. Для своего роста этот штамм нейроспоры мог использовать кинуренин или оксиантраниловую кислоту, но не использовал предшествующие метаболиты: индол, антраниловую кислоту и фенилаланин. Мутант, блокирующий синтез на стадии 3, накапливает индол и для роста использует триптофан, кинуренин и оксиантраниловую кислоту.
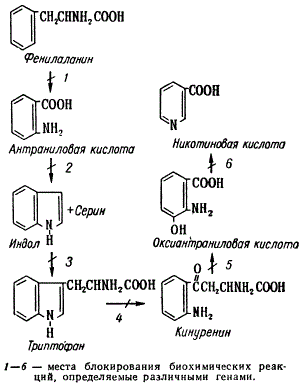
Схема биосинтеза триптофана и образования никотиновой кислоты у Neurospora
Он не может использовать только антраниловую кислоту и фенилаланин. Сопоставляя метаболические характеристики этих двух мутантов, не образующих никотиновой кислоты, можно определить, у какого из них ее синтез блокирован на более ранней ступени. Таким методом с использованием также других мутантов, нуждающихся в никотиновой кислоте, были выявлены все шесть представленных здесь ступеней метаболизма.
Приведенные наиболее простые примеры показывают лишь один из путей изучения действия гена методами биохимической генетики.
Мы уже говорили о том, что любой признак организма определяется многими генами, в конечном счете всем генотипом. С другой стороны, каждый ген обладает множественным, т. е. плейотропным, эффектом. Возможно, что величина плейотропного эффекта зависит от времени вступления гена в действие в ходе онтогенеза. Чем раньше вступает ген в действие, тем вероятнее, что он вызовет более глубокие биохимические изменения в последующем развитии и повлияет на многие признаки и свойства. На это указывает только что приведенный пример. Чем более ранний этап цепи биосинтеза блокируется, тем большее число метаболитов не сможет синтезироваться в клетке.
То, что установлено на нейроспоре, может показаться частным случаем.
Но такое представление было бы глубоким заблуждением. В настоящее время обнаружено, что ряд наследственных заболеваний у человека обусловлен врожденными пороками метаболизма. Эти заболевания касаются нарушений углеводного, жирового и белкового обмена веществ, приводящих к тяжелым последствиям. Мы приведем один из примеров генетически обусловленных нарушений биосинтеза у человека, сходных с тем, что установлено на нейроспоре.
Для нормального обмена веществ в организме человека необходимы аминокислоты, в частности определенные количества фенилаланина и тирозина. Обычно эти вещества получаются из пищи, а тирозин, кроме того, синтезируется в организме из избытков фенилаланина. В цепи биосинтеза тирозин либо служит предшественником для образования белков, некоторых гормонов (тироксин, норадреналин), меланина и др., либо распадается до углекислоты и воды.
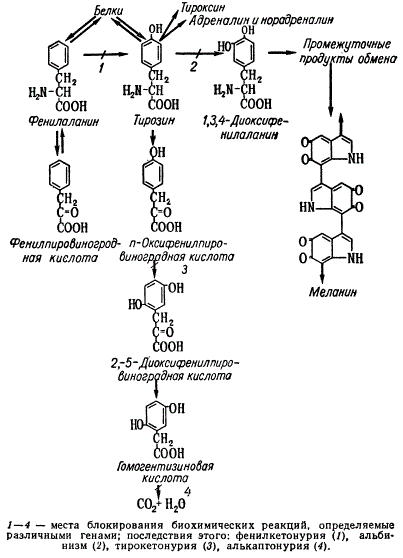
Схема фенилаланинтирозинового обмена у человека
Блокирование в результате биохимических мутаций какого-либо звена в цепи биосинтеза пигментов обусловливает их отсутствие — альбинизм, а также алькаптонурию и фенилкетонурию, которые являются наследственными болезнями человека. Так, например, альбинизм возникает в силу отсутствия меланина, который образуется в организме из тирозина через ряд сложных превращений, осуществляющихся в клетках — меланоцитах. Алькаптонурия обнаруживается по наличию у больных черного пигмента в моче, что вызывается окислением на воздухе гомогентизиновой кислоты. Фенилкетонурия наступает вследствие блокирования синтеза тирозина из фенилаланина. В результате этого в организме накапливается избыток фенилаланина, что вызывает у детей заболевание — умственную отсталость.
Знание механизма действия указанных генов, блокирующих определенные ступени цепи биосинтеза, дает возможность вырабатывать методы лечения или облегчения наследственных заболеваний. Например, у детей, у которых рано диагносцировали фенилкетонурию, удавалось предотвращать признаки умственной отсталости путем удаления из их пищи фенилаланина.
Таким образом, изучение генетиками конкретных путей осуществления действий гена может помочь медицине в решении одной из самых трудных ее задач — в разработке способов лечения различных наследственных болезней.
Биохимическая дифференцировка предшествует морфологической дифференцировке и морфогенезу. Однако изучение начальных биохимических этапов действия генов, направляющих дифференцировку и развитие морфологических структур, только начинается, и здесь требуются поиски новых путей и методов исследования. Поэтому генетики совместно с эмбриологами пошли по другому пути, а именно по пути исследования начального проявления мутантного признака в эмбриогенезе. Например, в работах Ю. А. Филипченко еще в 20-х годах изучалась эмбриология мутаций колоса пшеницы. Ф. Г. Добржанский установил плейотропный эффект гена white у дрозофилы, Н. Н. Медведев исследовал развитие имагинальных дисков трех мутаций глаза дрозофилы (eyeless, Lobe, Bar) в сравнении с развитием нормального глаза, Р. Гольдшмидт провел анализ развития мутаций крыла дрозофилы, и т. д. В этих и подобных исследованиях устанавливалось начало действия генов по отклонению от нормы в развитии определяемых ими признаков.

Проявление взаимодействия аллелей гена Т у мыши домовой
Для иллюстрации подобного подхода к изучению морфологического признака рассмотрим исследование мутаций у домашней мыши. Л. Денн с сотрудниками обнаружили серию множественных аллелей в локусе Т у домашней мыши. Доминантный ген Т в гомозиготном состоянии (ТТ) вызывает смерть зародыша на 11-й день. В гетерозиготном состоянии (Ttn) тот же ген сохраняет жизнеспособность, но вызывает укорочение хвоста — брахиурию (короткохвостость). Многочисленные рецессивные аллели этого локуса в различных сочетаниях в компаунде вызывают либо смерть зародышей на разных стадиях эмбриогенеза, либо развитие жизнеспособных с нормальными хвостами или бесхвостых мышей. Используя различные аллели, можно генетически моделировать продолжительность жизни эмбрионов и характер развития хвоста.
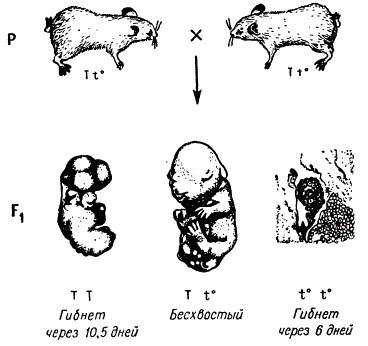
Схема наследования сбалансированных летальных факторов
Приведена схема наследования сбалансированных летальных факторов. В результате скрещивания Tt0 X Tt0 должны появиться три класса генотипов: TT, Tt0, t0 t0. Однако два из них не выживают. Гомозигота по доминантным аллелям ТТ гибнет на 10—11-й день развития, а по рецессивным аллелям t0t0 — на 5—6-й день. Эмбрион t0t0 гибнет вскоре после имплантации в результате нарушения развития мезодермы. В этой серии множественных аллелей была найдена еще одна рецессивная аллель t1, которая в зиготе действует на более ранней стадии — до имплантации яйца. В компаунде две аллели t0 t1 не летальны, а мыши этого генотипа имеют нормальные хвосты. Однако данное сочетание аллелей вызывает у самцов стерильность (самки фертильны); оно является также семилетальным, так как у эмбрионов этого генотипа часто развиваются уродства головы, что приводит к летальному исходу.
Из приведенного примера генетико-эмбриологического подхода к изучению действия гена видно, что комбинирование мутантных аллелей позволяет моделировать эмбриогенез, т. е. останавливать или изменять направление развития и уточнять начало дифференцировки того или иного признака.
