В 1898 году в Кавендишской лаборатории у Томсона закончил докторантуру сын новозеландского фермера Эрнест Резерфорд (1871—1937). Молодой физик получил назначение в Канаду, в Монреальский университет Мак-Гилла. В рекомендательном письме Дж. Дж. Томсон писал: «У меня никогда не было молодого ученого с таким энтузиазмом и способностями к оригинальным исследованиям, как г-н Резерфорд, и я уверен, что, если он будет избран, он создаст выдающуюся школу физики в Монреале…».
Ученик полностью оправдал надежды учителя. Монреальский период его работы славен не только выдающимися открытиями, но также началом, закладкой фундамента будущей школы новой физики.
О Резерфорде написано много прекрасных книг. Он прожил большую жизнь в науке, на самом переломе революции в физике. И создал свою научную школу. Правда, не в Монреале, а в Англии, куда вернулся в 1907 году.

Э. Резерфорд о период его работы в Монреале
Трудно найти в истории науки фигуру более симпатичную, чем этот огромный новозеландец с громовым голосом и тяжелыми кулаками фермера. Своими толстыми пальцами он умел так ловко пристроить невесомый листочек золота на опытную установку, что снискал себе славу лучшего экспериментатора в мире. Дело свое он совершал всегда с энтузиазмом и так заразительно, что невозможно было оставаться равнодушным.
В Монреале университетская лаборатория оказалась весьма неприспособленной для лелеемых Резерфордом замыслов. Но молодой ученый не унывал. «Я не теоретик, — любил он повторять и позже, собирая собственноручно приборы, необходимые для экспериментов. — Они играют в свои символы, а мы в Кавендише добываем неподдельные твердые факты природы». Резерфорд любил в шутку побахвалиться. На самом деле мало найдется ученых-экспериментаторов, кто столь тщательно бы заботился о том, чтобы его опыты были непременно подтверждены теорией, а его открытия имели бы строгое теоретическое обоснование.
В Монреале Резерфорд занялся исследованием радиоактивности урана и тория. Здесь он познакомился с талантливым химиком Фредериком Содди, с которым вместе открыл самопроизвольное превращение радиоактивных элементов. Здесь же, в университете Мак-Гилла, он впервые экспериментально подтвердил свое предположение, что альфа-частицы являются не чем иным, как атомами гелия, потерявшими два электрона. Впрочем, с точки зрения придирчивого экспериментатора, эти опыты пока не были достаточно убедительными. Можно смело сказать, что, работая в Монреале, Резерфорд создал учение о радиоактивности. Со временем Мак-Гиллский университет стал одним из крупнейших центров по изучению радиоактивности. А вокруг Резерфорда сплотилась большая группа молодых специалистов.
В 1905 году Резерфорду была присуждена в Англии почетная медаль Румкорфа. Молодого ученого избрали членом Лондонского королевского общества.
Два года спустя, распрощавшись с Канадой, Резерфорд уехал в Англию. Манчестерский университет предложил ему освободившуюся должность профессора физики. И здесь за какой-нибудь год образовался удивительный коллектив молодежи: студентов и аспирантов, таких же, как их шеф, бесконечно увлеченных физическими проблемами. Они много шутили, весело смеялись, но они очень много работали. Все жили в обстановке творческого подъема и не жалели для дела ни времени, ни сил.
Резерфорд придавал чрезвычайно большое значение исследованию альфа-частиц. Интуицией большого ученого он чувствовал, что им предстоит выдающаяся роль в нарождающейся атомной физике. И время показало, что он не ошибся.
Совместно с учениками Гейгером и Ройдсом Резерфорд проделал тончайшие измерения и определил более точно заряд и массу альфа-частиц, подтвердив, что они были не чем иным, как атомами гелия, потерявшими по два электрона. Атомы гелия, которые вылетали из урана и тория? Чудеса! Но эти «чудеса» ликвидировали все сомнения в правильности теории радиоактивного распада, которую он вместе с Содди выдвинул еще в Мак-Гиллском университете. Одновременно они требовали вплотную браться за исследование строения этих «кирпичей мироздания», чтобы ответить на недоуменные вопросы.
Альфа-частица — ядро атома гелия
Составляя программу работ в Манчестере, Резерфорд написал длинный список проблем, которые ему хотелось бы решить. Проблема под номером 7 называлась: «Рассеяние альфа-частиц». В Монреале ему так и не удалось понять, почему, пролетая сквозь слюду, альфа-частицы изменяли свою траекторию. Ответ на этот вопрос зависел от того, удастся или нет определить истинную конструкцию атома. Но как это сделать? И Резерфорд ответил на этот вопрос со свойственной ему решительностью: «Самый простой способ узнать, что находится внутри пудинга, — это сунуть в него палец!»
Он предложил Эрнсту Марсденну и Гансу Гейгеру поставить соответствующий эксперимент.
Установка молодых людей представляла собой нехитрое устройство, позволявшее обстреливать листочки тоненькой металлической фольги быстрыми альфа-частицами, вылетающими из кусочка радиоактивного вещества.
То было время, когда, как справедливо заметил писатель Митчел Уилсон, «если экспериментатор не мог поставить любой опыт с помощью обрывков веревки, нескольких палочек, резиновой полоски и собственной слюны, он не стоил даже бумаги, на которой пишет».
— Посмотрим: не сможете ли вы получить некий эффект прямого отражения альфа-частиц от металлической поверхности? — говорил шеф, осматривая установку.
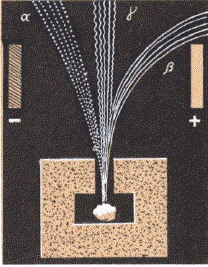
Схема разделения излучения по «сортам»
Такие эксперименты уже были раньше. Но Резерфорд чувствовал, что на этот раз опыт должен ему в чем-то помочь. Для Марсденна и Гейгера потянулись долгие часы томительного сидения в затемненной комнате. По редким вспышкам на светящемся экране нужно было подсчитывать число частиц, отклонившихся от своего пути после пролета через фольгу. В принципе они и должны были отклоняться, но отклоняться на малые углы. Ведь атом Томсона был электрически нейтрален. И пробить тоненький листочек золота альфа-частицам, по идее, действительно было не труднее, чем экспериментатору залезть пальцем в мягкий пудинг. И тем не менее молодые физики обнаружили, что некоторые альфа-частицы не только резко изменяли свой путь, пролетая через металл, но даже отскакивали от фольги обратно. Это «казалось столь же вероятным, — писал позже Резерфорд, — как если бы вы выстрелили 15-дюймовым снарядом в папиросную бумагу и этот снаряд отразился бы назад и попал в вас…»
Загадка стоила размышлений. И Резерфорд думал над ней упорно, настойчиво и долго. Думал везде. Думал, пока не пришел к удивительному выводу.
Если бы атомы представляли собой конструкции, предложенные Томсоном, альфа-частицы должны были бы свободно проходить через них, а следовательно, и через тонкую фольгу. Лишь отдельные «микроснаряды» могли чуть-чуть отклоняться, пролетая слишком близко возле «плавающих» в томсоновских атомах электронов и попадая в поле кулоновских сил. Но ни одна из пролетающих частиц не имела права отклоняться на те большие углы, которые наблюдали экспериментаторы, и тем более не могла отскакивать обратно.
В каком случае это было бы возможно? Только в том, если полный положительный заряд сосредоточен в центре, а не распределен по всему объему атома. Причем сосредоточен он должен быть в небольшом ядре. И между этим положительным ядром и отрицательно заряженными электронами должно быть достаточно большое свободное пространство.
Так Резерфорд пришел к ядерной модели атома.
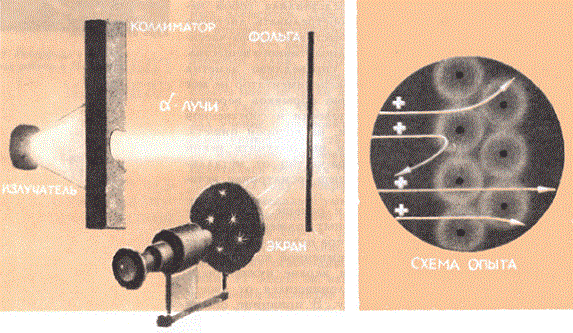
Схема опыта Резерфорда
Однажды вечером у себя в доме он собрал «мальчиков» и объявил, что знает, как выглядит атом…
Модель атома Резерфорда, как и модели его предшественников, походила на Солнечную систему. В центре сосредоточен весь положительный заряд атома, вся его масса — ядро. Вокруг ядра по постоянным орбитам, примерно так же, как планеты вокруг Солнца, обращаются отрицательные электроны. Сколько электронов на орбитах, столько и положительных зарядов в центральном ядре.
Но как быть с возражениями, погубившими аналогичную гипотезу Перрена и оставившими физиков равнодушными к модели Нагаоки?.. Резерфорд отвечал, ни минуты не задумываясь: никак! Эксперименты подтверждают догадку о том, что строение атома должно быть планетарным. А тот факт, что весь мир и Вселенная существуют и не развиваются, требует, чтобы такая конструкция атомов была устойчивой. Значит, так оно и есть! Что же касается теории, то со временем она появится.
В том же году в Брюсселе по инициативе и на средства богатого бельгийского промышленника Эрнста Сольвея собрался I Международный Сольвеевский конгресс. За немногим исключением, на него приехали все ведущие ученые в области теоретической и экспериментальной физики. Был на нем и Резерфорд.
В течение четырех дней за большим столом, за которым разместились все 27 участников конгресса, не прекращались споры. И самыми популярными словами были «квант» и «атом». Но что было самым удивительным — за все эти дни никто из присутствовавших ни разу не услышал громоподобного голоса Резерфорда. Это было на него так не похоже. И тем не менее это было так. Причина заключалась в том, что, упоминая атом, все выступавшие имели в виду модель Томсона и никто ни разу даже не упомянул об атоме Резерфорда. Ни для кого из них эта модель не имела ценности до тех пор, пока в основу ее не ляжет теория. Это сквозило в речах и Лоренца и Пуанкаре. Вин, Планк, Эйнштейн говорили только об атоме Томсона. А профессор Арнольд Иоганн Вильгельм Зоммерфельд (1868—1951) — маленький юркий человек, обладавший феноменальными математическими способностями, большим человеколюбием и педагогическим чутьем, — прямо заявил, что не желает даже слышать о каких-либо «частных моделях атомов».
Забегая вперед, скажу, что судьба посмеялась над Зоммерфельдом за эти слова. Мало кто из людей сделал больше, чем он, для утверждения квантовой модели атома Бора, являющейся разработкой модели Резерфорда.
Резерфорд молчал. Он лучше, чем кто-нибудь, видел недостатки своей модели и все-таки был уверен в ее истинности. «Вопрос об устойчивости предполагаемого атома на этой стадии не следует подвергать рассмотрению, ибо устойчивость окажется, очевидно, зависящей от тонких деталей структуры атома и движения составляющих его заряженных частей».
Эту фразу написал он в начале своей майской статьи. Этих же взглядов он продолжал придерживаться и теперь.
Вернувшись в Англию после рождества, Резерфорд приехал на ежегодный торжественный Кавендишский обед в Кембридж. В старинном зале, резные дубовые стены которого были увешаны портретами великих людей, вышедших из этого университета, собрались профессора и докторанты-стажеры. Представляя собравшимся Резерфорда, председатель упомянул о его великом открытии. Затем более подробно остановился на том, что никто из величайших физиков Кавендиша не смог бы соперничать с Резерфордом в тех виртуозных и изобретательных проклятиях, которыми сэр Эрнст награждал лабораторное оборудование.
Громкий хохот самого Резерфорда словно послужил сигналом к установлению сердечности на обеде. Гость из Манчестера много и увлеченно рассказывал о тех опытах, которыми заняты его молодые сотрудники. Все слушали внимательно. Но пожалуй, один человек слушал так, как никто. Он сидел на одной из задних скамей и, открыв рот, буквально впитывал в себя слова этого большого и добродушного человека, который был их гостем и чьи работы в Манчестере он хорошо знал.
Молодой человек, не сводивший с Резерфорда глаз, был Нильс Генрик Давид Бор. С первой же минуты встречи он почувствовал инстинктивное расположение и непреодолимую тягу к Резерфорду. И хотя учиться в Кавендишской лаборатории было и почетно и славно, тут же решил во что бы то ни стало перейти в Манчестер.
Бор был человеком осмотрительным. Он тщательно подготовил свой переход и примерно через год был уже в числе сотрудников Резерфорда.
