Примкнем к геологической экспедиции, выехавшей для исследования недр в один из районов нашей страны.
Экспедиция разбивается на отдельные партии — отряды.
Рано утром расходятся геологи по заранее намеченным маршрутам.
Геологи-разведчики при помощи буровых инструментов извлекают образцы пород из различных глубин земной коры и собирают на поверхности земли скальные породы.
Гидрогеологи занимаются исследованием водоносных горизонтов грунтовых и поверхностных вод. Вечером, вернувшись в свои походные палатки-лаборатории, они производят анализы добытых за день образцов.
Перед нами принесенные геологами образцы пород, содержащих кремний. Кремний по распространенности в природе занимает второе место, после кислорода. Около 30 процентов веса земной коры состоит из кремния. Но в природе кремний встречается не в свободном состоянии, а в соединении с кислородом (SiO2), которое химики называют кремнеземом, а геологи — кварцем.
Земная кора на 65 процентов состоит из кремнезема. Известны многочисленные разновидности этого соединения. Кремний, кварц, горный хрусталь, простой песок, точильный камень, различные драгоценные камни — все это родные братья кремнезема.
А как многообразно используется кремнезем в быту и в технике! Чайная и столовая посуда, сделанная из стекла, хрусталя, фарфора и фаянса, кирпичные здания, железобетонные сооружения и перекрытия, мосты, широкие полотна автострад, гранитные облицовки величественных зданий и набережных состоят главным образом из соединений кремния и кислорода.
Еще задолго до того, как человек начал использовать кремний в технике, в природе растения использовали его для своей жизни.
Прочность стебля растений обусловлена наличием в нем кремния и кислорода. В золе сгоревшей соломы или трубок бамбука мы находим много кремнезема, который при жизни растений настолько укрепляет их стебли, что они способны устоять против сильных порывов ветра и грозовых ливней.
Декоративные растения подкармливают специальными растворами солей кремнезема, чтобы укрепить их стебли и лепестки цветка. Такие растения можно перевозить на далекие расстояния.
Часто геологи-разведчики приносят с собой в палатку светлосерый камень — известняк, одну из кристаллических разновидностей углекислого кальция (СаСO3).
В состав углекислого кальция входит 48 процентов кислорода, 40 процентов кальция и 12 процентов углерода. Из этих же элементов состоят мел и мрамор — другие разновидности углекислого кальция.
Рассматривая известняк через лупу, иногда на его срезах можно заметить очертания раковин морских животных.
На необъятных просторах земли идет постоянный процесс превращения нерастворимого в простой воде углекислого кальция в растворимый. Потоки воды, насыщенные углекислым газом и содержащие углекислоту (Н2O+СO2— Н2СO3), встречают на своем пути углекислый кальций (СаСО3) и, вступая с ним во взаимодействие (СаСО3 + Н2СO3 — Са(НСO3)2), образуют соль, которая растворяется в воде и уносится в море. Для беспозвоночных животных, которые живут в морях и океанах, соли служат материалом для построения их наружного покрова — раковинок. Раковинки погибших животных скопляются на дне моря, постепенно образуя мощные слои известняка и мела.
Геологи считают, что те пространства земли, на которых сейчас встречаются огромные массивы известняка и мела, были когда-то морским дном.
При постройке зданий и сооружений известняк используется как строительный материал. Из известняка можно изготовить облицовочные плиты.
Большое количество известняка в Советском Союзе используется для получения другого ценного строительного материала — негашеной извести. Если углекислый кальций прокалить, он разлагается на известь и углекислый газ (СаСО3 — CaO + СO2). Всю негашеную известь и почти весь углекислый газ получают из известняка, прокаливая его в специальных печах.
Геологи-разведчики принесли в палатку-лабораторию образцы невзрачной на вид, но чрезвычайно ценной руды, состоящей из гидратов окиси алюминия: Аl(ОН)3 и Аl(ОН). Смесь этих кислородных соединений алюминия носит название бокситов. Они состоят из алюминия, водорода и кислорода. Из бокситов получают окись алюминия (А12O3), которую в технике называют глиноземом.
Глинозем является основным сырьем для производства алюминия.
Но чтобы получить алюминий, нужен еще и криолит — фтористая соль натрия и алюминия. Криолит в природе встречается редко, но его можно получить искусственным путем.
Алюминий получают электролизом в специальных ваннах, в которые загружают криолит и глинозем. Под действием постоянного тока температура в ванне повышается настолько, что криолит расплавляется. В расплавленной массе криолита растворяется глинозем. В растворе глинозема под действием постоянного электрического тока идет электролиз. Алюминий выделяется на графитовых стенках ванны, к которым подведен отрицательный полюс источника тока, а кислород, выделяясь на положительных графитовых электродах, постепенно сжигает их в двуокись углерода. На дне ванны скопляется расплавленный алюминий, который сливают через специальные отверстия.
Так из бокситов получают серебристо-белый металл, который обладает ценнейшими свойствами.
Сплав из 95 процентов алюминия и небольшого количества меди, магния и железа — дюралюмин — прочен, легок, почти в 3 раза легче железа. Дюралюмин покрывают очень тонким слоем чистого алюминия, чтобы предохранить его от разрушения на воздухе — коррозии. Это объясняется не тем, что алюминий вовсе не окисляется кислородом воздуха в присутствии влаги, а тем, что при своем окислении алюминий покрывается тонкой пленкой окиси, которая и предохраняет его от дальнейшего разрушения.
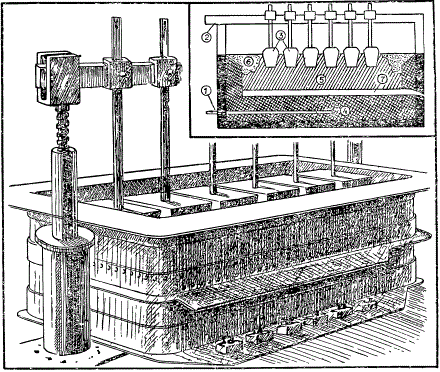
Ванна для получения алюминия электролизом: 1 — подвод тока к катоду; 2 — подвод тока к аноду; 3 — аноды; 4 — катоды; 5 — расплавленный электролит; 6 — застывший электролит; 7 — расплавленный алюминий.
Из алюминиевых сплавов изготовляют детали самолетов, части к автомобилям и другим машинам. Из них делают кухонную посуду, мебель, применяют в жилищном строительстве. Порошок алюминия входит в состав красок.
При нагревании алюминий жадно поглощает кислород, образуя окись алюминия. Реакция происходит с большим выделением тепла.
Этим свойством алюминия пользуются в технике.
Алюминиевый порошок смешивают с магнитной окисью железа (Fe3O4) и поджигают. Образуется высокая температура, при которой легко плавится металл. Такая смесь носит название термита и применяется для сварки трамвайных рельсов и других железных и стальных изделий.
Термит используется и для военных целей. Им заполняют специальные зажигательные артиллерийские снаряды и авиационные бомбы.
В виде металла алюминий нигде в природе не встречается. Но в различных кислородных соединениях он находится во всей земной коре.
Не вся земная кора доступна изучению. Современная геологическая техника позволяет исследовать ее на глубине 16—18 километров.
Алюминий составляет примерно 10 процентов веса земной коры, доступной исследованию. Он встречается не только в виде бокситов — он входит в состав глины, слюды и полевых шпатов. Во всех этих соединениях алюминий связан с кислородом.
Окись алюминия часто встречается в природе в виде минерала. К наиболее твердым минералам относится корунд, из которого изготовляют точильные камни и который входит в состав наждака.
Корунд и наждак — серые камки, мало привлекающие взгляд человека.
Встречаются и очень красивые природные драгоценные камни, состоящие из алюминия, кислорода и незначительной примеси хрома, титана или железа. Прекрасный рубин сверкает своим яркокрасным светом потому, что к природной окиси алюминия примешаны незначительные следы хрома. Такие же ничтожные количества других металлов, подмешанные к глинозему, превращают его в природе в зеленый изумруд или фиолетовый аметист.
Сейчас человек уже разгадал тайны природы и научился искусственным путем в специальных печах при высокой температуре изготовлять некоторые драгоценные камни, которые не только идут на украшения, но и применяются в технике.
В недрах земли находится еще одно кислородное соединение — магнитная окись железа (Fe3O4). В технике эту руду называют магнитным железняком. В земной коре его насчитывается до 5 процентов.
Магнитный железняк залегает огромными массивами. На Урале из него состоят целые горы: Магнитная, Высокая и Благодать. Руда эта составляет смесь закиси железа (FeO) и окиси (Fe2O3). Поэтому часто магнитный железняк называют закись-окись железа.
В природе часто встречается и другая разновидность железной руды — окись железа (Fe2O3), или красный железняк. Почти вся донецкая металлургическая промышленность снабжается этой рудой. Огромные запасы ее находятся в районе Кривого Рога и Курска.
Окись железа входит в состав бурого железняка — водной окиси железа бурого цвета. Залежи бурого железняка разрабатываются на Южном Урале, в Керчи и других местах Советского Союза.
СССР занимает первое место в мире по запасам железной руды. Больше половины всех мировых запасов железа падает на территорию Советского Союза.
В состав большинства полезных ископаемых, встречающихся в недрах земли, в том или ином виде входит кислород. Его можно встретить в химическом соединении с легкими элементами, включая магний и алюминий, в соединении с тяжелыми элементами, включая уран, с щелочными металлами — натрием и калием, с щелочноземельными металлами — кальцием, стронцием и барием и в соединении с редкими элементами.
Кислород — самый распространенный элемент на земле.
Много труда положили ученые, чтобы определить, сколько кислорода находится в природе. В настоящее время принято считать, что половину веса земной коры, воздуха, воды, животных и растительных организмов составляет кислород, а вторую половину — все остальные элементы периодической системы Менделеева.
