Свойством приспосабливаться обладает все живое (как на уровне организма, так и на уровне клетки).
В процессе приспособления изменяются биохимические процессы, функциональные свойства как клетки, так и организма. Функционирование отдельных клеток и поведение целого организма осуществляются на основе специфических механизмов.
Генотип, сложившийся под контролем естественного или искусственного отбора, определяет наследственную приспособленность организма к условиям внешней среды, в которой обычно осуществляется его онтогенез. Но так как факторы внешней среды разнообразны и изменчивы в довольно широких пределах, то в процессе эволюции отбор создает специальные механизмы индивидуального приспособления. Так, организмы одного генотипа могут легче, чем другие, приспосабливаться к понижению или повышению температуры, изменению давления, содержания кислорода в воздухе и т. д.
Способность организма приспосабливаться в индивидуальном развитии к меняющимся условиям окружающей его среды называют отногенетической адаптацией.
Организм может адаптироваться как к постоянно, систематически действующим в течение индивидуальной жизни факторам внешней среды, так и к флуктуирующим.
Онтогенетическая адаптация может быть генотипической и фенотипической. Генотипическая адаптация представляет собой наследственно детерминированное в результате отбора приспособление организма к конкретным условиям внешней среды. Фенотипическая адаптация хотя и не сопровождается наследственным изменением, тем не менее, ограничена в своих пределах нормой реакции генотипа.
С одной стороны, онтогенетическую адаптацию условно подразделяют на тканевую (клеточную) и организменную, или «системную», адаптацию, относящуюся к приспособлению целого организма. С другой стороны, онтогенетическую адаптацию можно подразделять на субстанциональную и функциональную. В случае субстанциональной адаптации к воздействию токсичного агента повышается порог денатурации белков протоплазмы, возбудимости и наступления смерти клетки. При функциональной адаптации происходит изменение функций клетки, ткани, органа или целого организма.
Клеточную, или тканевую адаптацию можно иллюстрировать многочисленными примерами. В случае гипоксии — кислородного голодания — в организме теплокровных животных происходит увеличение числа эритроцитов и изменение биохимических процессов в клетках. Приучение изолированной мышечной ткани лягушки (или целого организма) к высокой температуре вызывает в ее клетках повышение порога денатурации белка при действии высокой температуры. Предварительное приучение инфузорий к различным токсичным растворам, повышенной солености, крайним температурам повышает их устойчивость к этим агентам. При этом в случае бесполого размножения приобретенные свойства могут сохраняться длительное время. Такие адаптивные изменения, сохраняющиеся длительное время в ряду бесполых поколений, В. Иоллосом были названы длительными модификациями.
В опытах Ю. И. Полянского и А. Ф. Орловой клоны инфузорий в течение 3—8 недель содержались при трех разных температурах: 12—13, 18—20 и 24—26°. Затем сравнивалась продолжительность выживания этих инфузорий при температуре 40°. Инфузории, предварительно содержавшиеся при повышенной температуре, жили при 40° более длительное время. Приобретенная теплоустойчивость может сохраняться неделями при бесполом размножении, но затем исчезает, что указывает на ее нестойкий характер. Длительные модификации могут иметь огромное приспособительное значение для животных, растений и микроорганизмов.
У микроорганизмов в особенности важно отличать фенотипическую адаптацию от генотипической, вызванной отбором мутаций. Благодаря тому, что у них происходит частая смена поколений, возникающие мутации могут быстро подхватываться отбором и размножаться в популяции, создавая генотипическую адаптацию, которую в данном случае трудно отличить от фенотипической. Поэтому при наличии полового размножения для различения генотипической и фенотипической адаптаций необходимо проводить скрещивание или использовать специфические методы анализа.
В процессе клеточной фенотипической адаптации происходит изменение метаболических процессов. Примером этому может служить опыт с адаптацией дрожжей (Saccharomyces cerevisiae) к галактозе.
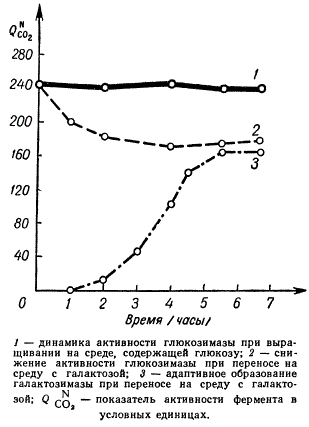
Адаптация дрожжей к сбраживанию галактозы
Обычно этот вид дрожжей выращивают на среде, содержащей глюкозу, которая и сбраживается дрожжами. Если клетки дрожжей, выращенных на глюкозе, отмыть и перенести в среду, лишенную глюкозы, но содержащую галактозу, то дрожжи вначале не размножаются. Однако через несколько часов они все же приобретают способность сбраживать галактозу, так как у них происходит перестройка гликолитического механизма. Эта перестройка у дрожжей представляет не генотипическую (за счет отбора мутантов), а фенотипическую адаптацию. Если в питательную среду прибавляют глюкозу, то клетки теряют приобретенную адаптацию и переключаются на сбраживание глюкозы. Подобные опыты указывают на то, что в процессе адаптации происходит синтез специфического фермента или набора ферментов, осуществляющих сбраживание необычного субстрата. Адаптационные изменения ферментативной деятельности называют ферментативной адаптацией. Ферментативная адаптация обеспечивается генетическими механизмами регуляции синтеза ферментов.
Наиболее отчетливо существование механизмов онтогенетической адаптации можно видеть у многоклеточных организмов, в особенности у животных. Прежде всего, к ним относятся физиологические механизмы, обеспечивающие сохранение постоянства внутренней среды организма. Многоклеточный организм обладает также рядом других механизмов приспособления: 1) регенерацией тканей и функциональным замещением (компенсацией) утраченной функции, 2) иммунитетом, обеспечивающим устойчивость организма против инородных включений, в том числе против инфекционных начал, 3) функциональной адаптацией органов в зависимости от влияния внешних раздражителей на организм. В качестве примера рассмотрим здесь иммунитет.
Иммунитетом в широком смысле слова обладают все организмы — животные, растения и микроорганизмы. Иммунитет может быть врожденным (генотипическим) и приобретенным (фенотипическим). Проникновение в организм чужеродного белкового тела, являющегося антигеном, ведет к выработке в крови животного соответствующих антител, которые делают организм невосприимчивым, устойчивым к этому антигену или сходному с ним. Мобилизация защитных иммунологических механизмов против заражения паразитами, бактериальной или вирусной инфекции является одним из общих и важных адаптационных механизмов в онтогенезе. На введенный белок в организме вырабатываются соответствующие антитела. Благодаря этому в ряде случаев в организме обеспечивается иммунологическая память, т. е. защита от инфекции.
Своеобразным примером иммунитета может служить явление резус-фактора, приводящего к несовместимости крови матери и ребенка. Эритроциты большинства людей агглютинируются сывороткой от кроликов, иммунизированных кровью обезьян макака-резус, эритроциты других — не агглютинируются. Антиген, ответственный за выработку антитела у иммунизированных кроликов, вызывающих агглютинацию эритроцитов у человека и обезьян, и был назван резус-фактором. Людей, обладающих этим фактором, называют резус-положительными (Rh+), а людей, не обладающих этим фактором, — резус-отрицательными (Rh—). Резус-фактор определяется доминантным геном Rh, отсутствие его — рецессивной аллелью этого гена rh.
Если мать и отец являются резус-положительными или оба резус-отрицательными, то заболевание крови младенца не наступает. Указанной болезнью страдают младенцы, происходящие только от резус-положительного отца и резус-отрицательной матери.
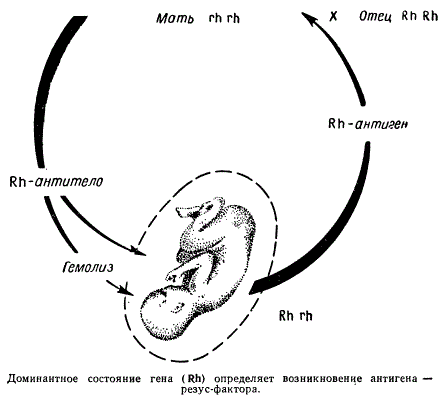
Взаимоотношение матери и эмбриона при несовместимости их по резус-фактору
Схематически изображено взаимоотношение генотипа (эмбриона и матери) в отношении резус-фактора. Эмбрион является гетерозиготой по резус-фактору (Rh rh), поэтому он обладает способностью вырабатывать антиген, который через плаценту попадает в кровь матери. В крови резус-отрицательной матери против антигенов резус-положительного эмбриона вырабатываются антитела. Антитела, попадая в кровь эмбриона, вызывают у него частичную агглютинацию эритроцитов, что и приводит к гемолизу крови, обусловливая анемию у ребенка.
При первой беременности не всегда успевает выработаться большое количество антител, поэтому первый младенец страдает в меньшей мере. Но во время второй беременности при развитии эмбриона того же генотипа в крови матери накапливается достаточно много антител, что может вызвать гибель эмбриона.
Сходное явление выработки антител в крови материнского организма на антигены плода обнаружено у многих животных: крупного рогатого скота, лошадей, свиней, кур, собак, кошек, кроликов, морских свинок. У кур антитела, выработанные в материнском организме, попадают не в зародыш яйца, а в белок. При развитии цыпленка антитела попадают из белка в зародыш, обусловливая «врожденную» анемию крови.
Материнский организм, благодаря такой иммунной реакции, спасает себя от губительного действия антигена, определяемого генотипом зародыша. Зная генетическую и иммунологическую причину этого явления, можно предупреждать при бракосочетании отрицательные последствия, разрабатывая меры по спасению ребенка, что теперь и практикуется.
Описанное явление служит примером генотипической адаптации, так как адаптивная реакция — выработка антител так же, как и образование антигенов, обусловливается определенными генотипами. При обычных прививках, которые проводятся в профилактических целях, в организме вырабатывается временный иммунитет, но он не является наследственным. Его возникновение служит примером фенотипической адаптации.
