Уже давно было подмечено, что лишенные окраски клетки и органы растения (например, корни) не способны фотосинтезировать. Особенно наглядны в этом отношении альбиносы (от лат. альбус — белый) — неокрашенные проростки, развивающиеся иногда у высших растений даже при хорошем освещении. Отсутствие окраски вызывается у таких растений какими-то внутренними факторами, препятствующими образованию особых красящих веществ — пигментов (от лат. пигментум — краска) при самых благоприятных для этого внешних условиях. При полном альбинизме, который довольно часто можно наблюдать у кукурузы, проростки не способны осуществлять фотосинтез и поэтому погибают от истощения вскоре после появления двух или трех листочков. Частичный альбинизм обычно встречается при пестролистности, когда белыми и не способными к фотосинтезу оказываются отдельные участки листа. Пестролистные формы отличаются своеобразной красотой и в связи с этим широко используются как декоративные растения.
Явление альбинизма у растений свидетельствует об огромной роли пигментов для фотосинтетической деятельности. Установлено, что процесс фотосинтеза связан прежде всего с поглощением света пигментами пластид. Энергия солнечной радиации сможет превратиться в химическую энергию образующихся при этом органических веществ только в том случае, если она сначала будет поглощена пигментами фотосинтезирующих систем и в первую очередь зеленым пигментом — хлорофиллом.
Пигменты фотосинтезирующих систем можно разделить на три основные группы: хлорофиллы, каротиноиды и фикобилипротеиды. Пигментный состав различных фотосинтезирующих систем неодинаков и зависит от принадлежности растения к той или иной систематической группе.
Важнейшие представители пигментов фотосинтезирующих систем у различных групп растений
| Пигменты | Серобактерии | Водоросли | Высшие растения | |||||
| пурпурные | зеленые | сине-зеленые | красные | диатомовые | бурые | зеленые | ||
| Хлорофиллы | ||||||||
| хлорофилл a | — | — | + | + | + | + | + | + |
| хлорофилл b | — | — | — | — | — | — | + | + |
| хлорофилл c | — | — | — | — | + | + | — | — |
| хлорофилл d | — | — | — | + | — | — | — | — |
| бактериохлорофилл | + | — | — | — | — | — | — | — |
| бактериовиридин | — | + | — | — | — | — | — | — |
| Фикобилипротеиды | ||||||||
| фикоэритрин | — | — | + | + | — | — | — | — |
| фикоциан | — | + | + | — | — | — | — | |
| Каротиноиды | ||||||||
| β-каротин | — | — | + | + | + | + | + | + |
| лютеин | + | — | — | + | + | |||
| виолаксантии | — | — | — | + | + | + | ||
| фукоксантин | — | — | — | ? | + | + | — | — |
Условные обозначения:
+ наличие пигмента; — отсутствие; ? — очень малое количество; пустые клетки — не было исследований.
Для обозначения различных форм хлорофилла используются буквы латинского алфавита: а, b, с, d.
Из таблицы видно, что среди различных форм хлорофилла наибольшее распространение имеет хлорофилл a — обязательный компонент пластид всех фотосинтезирующих растений. Хлорофилл a отсутствует у пурпурных и зеленых серобактерий, для которых характерна наиболее примитивная форма синтеза органических веществ, так называемый бактериальный фотосинтез или фоторедукция. Эти бактерии восстанавливают CO2 в анаэробных условиях до уровня органических веществ за счет энергии солнечного света с использованием сероводорода или некоторых других неорганических веществ, при этом не происходит выделения молекулярного кислорода. Вместо хлорофилла a пурпурные серобактерии содержат бактериохлорофилл, а зеленые серобактерии — бактериовиридин.
Строение пигментов
Изучение химических свойств хлорофилла a позволило расшифровать его структуру. Правильность предложенной структурной формулы подтверждена полным синтезом хлорофилла, осуществленным в 1960 г. почти одновременно в лабораториях М. Штрелля и Р. Вудварда. Основу молекулы хлорофилла составляют четыре пиррольных кольца (I, II, III и IV). Пиррол представляет собой пятичленное циклическое соединение. Остатки пиррольных колец, соединяясь между собой, образуют ядро молекулы хлорофилла, в центре которого помещается атом магния. Он соединяется с азотом пиррольных колец, причем два атома азота соединяются с магнием своими основными валентностями, а два других — дополнительными валентностями. Зеленый цвет хлорофилла как раз и определяется наличием металла в его молекуле. В этом легко убедиться, стоит только осторожно подействовать на спиртовую вытяжку хлорофилла кислотой. Магний замещается двумя атомами водорода из кислоты и получается бурый продукт — феофитин. Восстановить зеленый цвет вытяжки можно путем добавления какой-либо соли магния или другого двухвалентного металла.
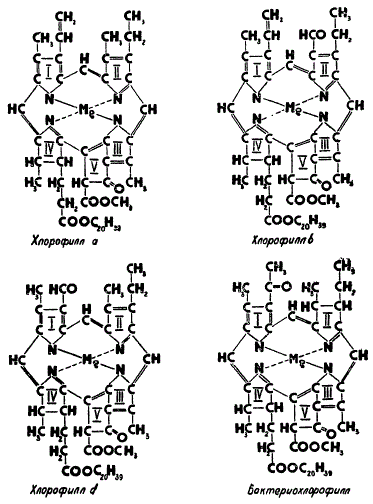
Структура хлорофиллов
Одной из специфических черт хлорофиллов является наличие в их молекуле добавочного кольца из пяти углеродных атомов (V). Кислотная, или карбоксильная, группа (—СООН) этого кольца соединена эфирной связью с метиловым спиртом (СН3ОН). Вторая карбоксильная группа, находящаяся около четвертого пиррольного кольца, соединена эфирной связью с другим спиртом — фитолом (С20Н39ОН).
Таким образом, по своей химической природе хлорофилл (см. его структурную формулу на обложке книги) — сложный эфир двухосновной кислоты хлорофиллина, в одном карбоксиле которой водород замещен остатком метилового спирта (—СН3), а в другом — остатком фитола (—С20Н39).
Интересно отметить, что наличие остатка фитола обусловливает липофильность молекулы хлорофилла, проявляющуюся в его растворимости в жировых растворителях. Кроме того, остаток фитола играет существенную роль в образовании комплексов хлорофилла с липоидами. Выделенный в чистом виде фитол напоминает бесцветную воскообразную массу.
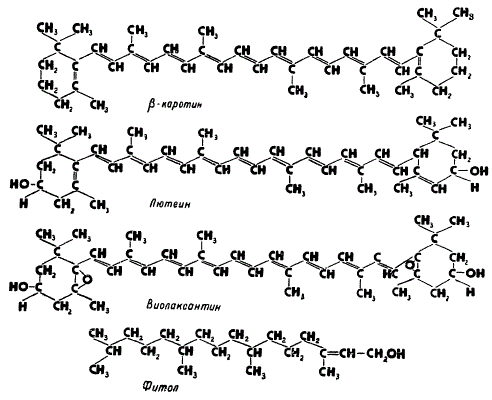
Структура фитола и каротиноидов
По своей химической природе хлорофилл весьма близок к некоторым важным дыхательным ферментам, а также к красящему веществу крови — гему гемоглобина. Общность химической природы двух основных пигментов живых организмов, а именно хлорофилла растений и гемоглобина животных, заключается в том, что у гема также имеется ядро, состоящее из четырех соединенных друг с другом пиррольных колец, в центре которого находится атом металла, только у хлорофилла — это магний, а у гема — железо. Исследования С. Граника, Т. Н. Годнева и других ученых показали, что биосинтез хлорофилла и гема осуществляется на начальных этапах аналогичным путем из одних и тех же веществ. Эти факты сходства в строении в способе образования хлорофилла и гема гемоглобина еще раз указывают на родство происхождения столь отдаленных организмов, как растения и животные.
Помимо хлорофилла a, обладающего сине-зеленой окраской, в хлоропластах зеленых водорослей и высших растений обнаружена еще другая форма желто-зеленого цвета — хлорофилл b. В отличие от хлорофилла a, имеющего эмпирическую формулу C55H72O5N4Mg, хлорофилл b содержит лишь на два атома водорода меньше и на один атом кислорода больше. В структурном отношении это незначительное различие сводится к тому, что вместо метильной группы (—СН3) при втором пиррольном кольце у хлорофилла b имеется альдегидная группа COH. Красные водоросли содержат два зеленых пигмента: хлорофиллы a и d, очень близкие по структуре. Они различаются только тем, что у хлорофилла d при первом пиррольном кольце стоит не винильная группа (—СН = СН2), а альдегидная. У бурых и диатомовых водорослей вместо хлорофилла b содержится хлорофилл с, который в отличие от других форм лишен остатка фитола.
Пурпурные серобактерии имеют весьма близкий к хлорофиллу a бактериохлорофилл. Небольшое различие состоит в том, что у этого пигмента при первом пиррольном кольце находится вместо винильной ацетильная группа (—СО—СН3), а также на два атома водорода больше во втором пиррольном кольце. Характерный для зеленых серобактерий бактериовиридин (иногда его называют хлоробиум-хлорофиллом) изучен пока недостаточно полно, состав и строение окончательно еще не установлены. Известно только, что он не дает характерных реакций на присутствие в его молекуле пятого кольца и содержит вместо фитола транс-фарнезол (C15H26O).
Наряду с хлорофиллами к постоянным компонентам комплекса пигментов фотосинтезирующих систем относятся каротиноиды. Обычно это желтые, оранжевые и светло-красные пигменты, которые хорошо растворяются в жирах и растворителях жиров, но не растворяются в воде. Как правило, их окраска маскируется интенсивным зеленым цветом хлорофиллов. Поэтому в природе только осенью, когда преимущественно происходит разрушение зеленых пигментов, листья желтеют и каротиноиды становятся доступными для непосредственного наблюдения.
К основным каротиноидам пластид относятся каротины, представляющие собой ненасыщенные углеводороды (эмпирическая формула C40H56), и их кислородсодержащие производные — ксантофиллы.
Молекулы большинства каротиноидов имеют вид длинной углеродной цепи, которая часто заканчивается на одном или на обоих концах кольцом ионона. Атомы углерода соединяются друг с другом в длинную цепь посредством чередующихся одинарных и двойных связей. Такие связи называются конъюгированными, их наличие в молекуле обусловливает характерную окраску каротиноидов.
Пластиды высших растений и большинства водорослей содержат до восьми и больше различных каротиноидов. Кратко остановимся на характеристике некоторых из них.
Типичными, широко распространенными каротиноидами высших растений являются β-каротин, лютеин и виолаксантин. β-каротин — это желто-оранжевый пигмент. Название его происходит от латинского слова карота — морковь, в корнях которой отлагается значительное количество его в виде желто-оранжевых кристаллов. К β-каротину близок по составу и структуре лютеин. Это желтый пигмент из группы ксантофиллов, представляющий собой двухатомный спирт с эмпирической формулой С40Н56О2, причем обе спиртовые группы (—ОН) находятся в кольцах ионона. Другим близким к лютеину пигментом из группы ксантофиллов является виолаксантин с эмпирической формулой С40Н56О4. Он имеет в своем составе на два атома кислорода больше, чем лютеин. Установлено, что эти два атома кислорода входят в состав иононовых колец в виде добавочных эпокси-группировок (> O), отличающихся большой лабильностью и реакционной способностью.
К группе ксантофиллов относится также и фукоксантин (от лат. фукус — род бурых водорослей и от греч. ксантос — желтый), встречающийся у бурых и диатомовых водорослей. Он имеет оранжево-бурый цвет, близок по своим свойствам к лютеину и виолаксантину, однако состав и структура его окончательно еще не выяснены, поэтому в эмпирической формуле (С40Н54-60О6) указывается возможное количество атомов водорода.
Набор каротиноидов в хроматофорах фоторедукторов (пурпурные и зеленые серобактерии) существенно отличается от такового в хлоропластах фотосинтетиков. Для фоторедукторов характерно отсутствие пигментов из группы ксантофиллов, содержащих эпокси-группировки. Основным каротиноидом зеленых серобактерий оказался желтый пигмент, γ-каротин, у которого имеется только одно иононовое кольцо. Что касается пурпурных серобактерий, то у них широко распространены ликопин и другие близкие к нему каротиноиды ациклического типа, не имеющие в своем составе ни одного иононового кольца.
Помимо хлорофиллов и каротиноидов, красные и сине-зеленые водоросли содержат еще дополнительные пигменты, хорошо растворимые в воде, так называемые фикобилипротеиды, к которым относятся фикоэритрины (красного цвета) и фикоцианы (сине-фиолетового цвета). Само название указывает на то, что в химическом отношении эти пигменты представляют собой сложные белки — протеиды. Небелковыми компонентами у них служат обусловливающие окраску фикобилины, которые связываются с белками в сложные комплексы. Связь небелковой группы с белком настолько прочна, что отделить фикобилины от белка можно лишь путем кипячения с сильными кислотами.
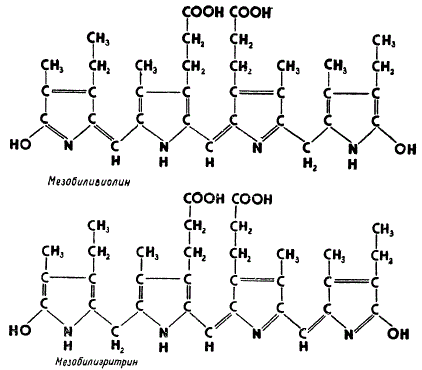
Структура фикобилинов
Небелковым компонентом у фикоэритринов является мезобилиэритрин, а у фикопианов — мезобиливиолин, структура которых представлена на рисунке. Как видно, фикобилины имеют в своем составе четыре пиррольных кольца, соединенных друг с другом в виде развернутой цепи, однако в деталях структура их окончательно еще не установлена. Важно подчеркнуть, что фикобилины весьма близки по своей химической природе к желчным пигментам животных.
Содержание пигментов
Теперь кратко остановимся на вопросе о количественном содержании основных представителей различных групп пигментов и о их соотношении. Общее количество хлорофилла невелико и составляет в среднем около 1 % от сухого вещества листа, но оно может сильно варьировать, изменяясь у водорослей от 0,6 до 1,5%, а у высших наземных растений от 0,7 до 1,3%. Даже в пределах одного и того же растения разные листья часто значительно отличаются по содержанию зеленых пигментов, Хрофилла а всегда больше, на три его молекулы обычно приходится одна молекула хлорофилла b. Однако у теневых листьев и теневыносливых растений хлорофилла b больше, чем у светолюбивых. Так, у многих зеленых водорослей, произрастающих в условиях сильного затенения, среднее отношение хлорофилла a к хлорофиллу b снижается до 1,4. Вместе с тем их соотношение у исключительно светолюбивых растений в среднем доходит до 5,5.
В нормально развитых листьях каротиноидов гораздо меньше, чем. зеленых пигментов, примерно в 3—5 раз, а иногда даже еще меньше. Отношение же ксантофиллов к каротину может изменяться в зависимости от вида растений и условий их произрастания в очень широких пределах, от 1,8 до 15, но в среднем оно таково, что на 2—3 молекулы ксантофиллов приходится одна молекула каротина.
По данным В. Н. Люб именно, отношение фикоэритрина к хлорофиллу колеблется у разных видов красных водорослей от 0,06 до 0,66. Содержание фикоэритрина возрастает с увеличением глубины обитания этих водорослей. В среднем на одну квантосому приходится 230 молекул хлорофилла и 48 молекул каротиноидов.
Оптические свойства и состояние пигментов
Глубоко понять механизм процесса фотосинтеза возможно лишь на основе современных представлений о физических свойствах пигментов и их состоянии в живой клетке. Основная функция пигментов фотосинтезирующих систем заключается в поглощении света. Отсюда понятно то исключительно важное значение, какое имеет познание оптических свойств различных пигментов и в первую очередь их спектров поглощения.
Поглощение световой энергии пигментами осуществляется не сплошным, а избирательным образом и зависит от структуры молекулы данного пигмента. Явление это может наблюдаться как в видимой части солнечного спектра, так и в невидимых участках (инфракрасном и ультрафиолетовом), однако особый интерес представляют спектры поглощения пигментов только в интервале фотосинтетически активной радиации (380—720 ∙ 10-9 м).
Хлорофиллы a, b, с, d, а также бактериовиридин имеют два основных максимума поглощения в красной и сине-фиолетовой частях спектра с незначительными различиями в их положении. Как видно на рисунке, у хлорофилла b максимум поглощения в красной части спектра несколько смещен в сторону коротковолновых лучей, а в сине-фиолетовой части, наоборот, в сторону длинноволновых лучей по сравнению с положением аналогичных максимумов у хлорофилла а.
Спектры поглощения растворов зеленых пигментов показывают, что сине-фиолетовые и красные лучи поглощаются интенсивно, тогда как зеленые и желтые — очень слабо, поэтому последние хорошо проходят через эти пигменты, обусловливая их цвет. Поскольку желтые лучи маскируются зелеными, окраска хлорофилла получается зеленая. Однако тот же самый раствор хлорофилла, имеющий в проходящих лучах зеленую окраску, в отраженном свете воспринимается как вишнево-красный благодаря явлению флуоресценции.
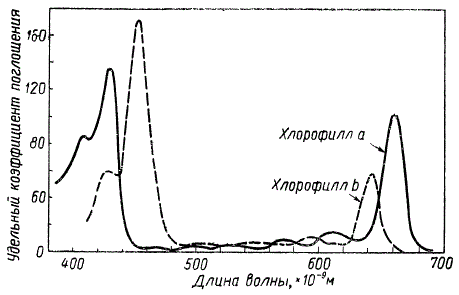
Графическое сравнение спектров поглощения хлорофилла а и b в эфирных растворах (по Цшейле)
Флуоресценция (от англ. флуэреснт — свечение) представляет собой кратковременное свечение, прекращающееся практически одновременно с прекращением освещения данного вещества. Способность к такого рода свечению является очень важным оптическим свойством зеленых пигментов, указывающим на их значительную фотохимическую активность. Это свойство гораздо лучше обнаруживается не на живых листьях, а на растворах зеленых пигментов, потому что свечение хлорофилла, находящегося в клетках листа, примерно в 10 раз слабее, чем в растворе. Красное свечение хлорофилла легко наблюдать, если рассмотреть его вытяжку (например, спиртовую) со стороны падающего света, а за пробиркой с вытяжкой поместить черный фон, поглощающий все проходящие через нее лучи. При этом естественно возникает вопрос: почему окраска вытяжки хлорофилла в отраженном свете не такая, как в проходящем? Постараемся кратко объяснить это.
Свет поглощается дискретно, т. е. порциями в виде квантов, или фотонов. Энергию кванта (Е) можно выразить, как E = h ∙ v, где h — постоянная Планка, v — частота колебаний света, обратно пропорциональная длине волны. В основном, устойчивом состоянии молекулы хлорофилла каждый электрон находится на определенном энергетическом уровне и обладает соответствующим запасом энергии. Поглощение кванта света приводит к переходу электрона на более высокий энергетический уровень, при этом молекула становится возбужденной с избыточным количеством энергии. Однако время, в течение которого молекула существует в возбужденном состоянии, чрезвычайно мало, примерно 10-9 сек, а следовательно, возбужденное состояние неустойчиво и вскоре происходит возвращение молекулы к более устойчивому состоянию с меньшим запасом энергии, или к исходному. Возбужденная молекула может терять энергию несколькими путями, наиболее важным из которых является путь превращения этой энергии в химическую энергию. Кроме того, энергия возбужденной молекулы может либо рассеиваться в виде тепловой энергии как внутримолекулярным, так и межмолекулярным путем, либо испускаться в виде кванта света. При флуоресценции возбужденные молекулы испускают кванты света, обладающие меньшей энергией, а значит, большей длиной волны по сравнению с теми квантами, которые вызывают это свечение. Каждое вещество испускает лучи определенной длины волны, т. е. имеет свой специфический спектр флуоресценции. По таким спектрам можно довольно легко отличить одно флуоресцирующее вещество от другого.
Спектр флуоресценции хлорофилла имеет только один основной максимум свечения, приходящийся на более длинноволновую красную область спектра в сравнении с максимумом поглощения в этой же области. Это значит, что при флуоресценции хлорофилл всегда испускает только длинноволновые красные лучи даже в том случае, когда он освещается синими или фиолетовыми лучами. Вот почему вытяжка хлорофилла имеет в отраженном свете темно-красную окраску.
Кроме зеленых пигментов, флуоресцировать способны и фикобилипротеиды, причем фикоциан в растворе обнаруживает красное свечение, фикоэритрин — оранжевое. Каротиноиды же обычно считаются не способными к флуоресценции.
Ученых давно интересовало, в каком состоянии находится хлорофилл в хлоропласте. Особое состояние пигментов в живой клетке убедительно доказывается, в частности, несовпадением их оптических свойств со свойствами растворов тех же самых пигментов, например несовпадением спектров поглощения, а также спектров флуоресценции. Максимумы поглощения хлорофиллов и ряда других пигментов, находящихся в живой клетке, оказываются сильно сдвинутыми в длинноволновую область по сравнению с максимумами поглощения света растворами этих пигментов. Так, раствор бактериохлорофилла имеет в инфракрасной области спектра только один максимум поглощения при 770—780 ∙ 10-9 м (7700—7800 Å), тогда как этот же пигмент, но находящийся в клетках пурпурных серобактерий, обнаруживает три максимума поглощения, причем все они приходятся на более длинноволновый участок инфракрасных лучей: 800, 850 и 890 ∙ 10-9 м (8000, 8500 и 8900 Å). Максимум флуоресценции бактериохлорофилла живых клеток также значительно сдвинут в длинноволновую часть и приходится на 900—920 ∙ 10-9 м вместо 780—790 ∙ 10-9 м — положения максимума флуоресценции этого пигмента в растворе.
До недавнего времени широкое распространение имело положение, высказанное крупнейшим специалистом в области фотосинтеза В. Н. Любименко, что особое состояние зеленых пигментов в живой клетке обусловливается связью их с белками. Однако сейчас накопилось достаточно экспериментальных данных, свидетельствующих о том, что специфику оптических свойств хлорофиллов живых клеток недостаточно объяснить только связью их с белками. А. А. Красновский, Т. Н. Годнев и другие установили возможность существования одного и того же пигмента живой клетки в нескольких формах, причем некоторым из них свойственно агрегированное состояние с разным характером упаковки молекул. Оказалось, что положение максимумов поглощения на спектрах хлорофилла а, бактериохлорофилла и бактериовиридина зависит от характера агрегации. В качестве примера, иллюстрирующего влияние агрегации пигмента на его спектры, приведем результаты опытов по изучению бактериохлорофилла, находящегося в живых клетках (пурпурные бактерии) и модельных системах; эти опыты проведены А. А. Красновским с сотрудниками. В некоторых случаях модельными системами служили твердые пленки, которые получались путем выпаривания эфирного раствора бактериохлорофилла в вакууме, т. е. в условиях, заведомо содействующих агрегации молекул пигмента.
Хорошее совпадение спектров поглощения и спектров флуоресценции твердых пленок этого пигмента с соответствующими спектрами пурпурных бактерий указывает на наличие в живых клетках агрегированных форм бактериохлорофилла. В настоящее время считается, что пурпурные бактерии содержат три различно агрегированные формы зеленого пигмента. В соответствии с положением основных максимумов поглощения в инфракрасной части спектра при 800, 850 и 890 ∙ 10-9 м эти формы бактериохлорофилла принято обозначать как Б800, Б850 и Б890.
Проблема множественности форм хлорофилла приобрела исключительно важное значение после того, как было установлено, что первичный процесс фотосинтеза включает в себя не одну фотохимическую реакцию, а две и что различные формы пигмента могут осуществлять самостоятельно специфические функции.
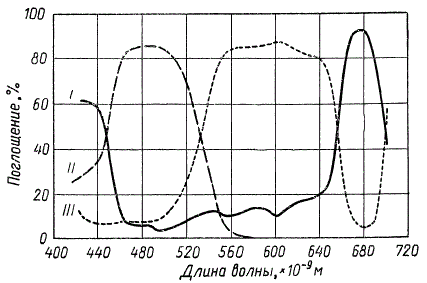
Графическое сравнение спектров поглощения пигментов сине-зеленой водоросли Chroococcus (по Р. Эмерсону): I — хлорофилл; II — каротиноиды; III — фикоциан
Спектры всех каротиноидов в видимой области характеризуются двумя или тремя интенсивными полосами поглощения в сине-фиолетовой части. Спектры поглощения фикоэритрина и фикоциана близки между собой, их максимумы приходятся на зеленую и желтую части спектра, располагаясь между двумя основными полосами поглощения зеленых пигментов. Это позволяет считать, что фикобилипротеиды наряду с каротиноидами являются дополнительными пигментами к хлорофиллу.
Адаптация к условиям освещения
Фикоциан и фикоэритрин как дополнительные пигменты играют существенную роль в адаптации (приспособлении) растений к условиям освещения, обеспечивая наилучшее использование солнечной энергии для фотосинтеза.
Адаптацию к качеству и интенсивности света можно наглядно видеть на примере вертикального распределения морских водорослей в зависимости от их окраски: в самых поверхностных слоях воды преобладают зеленые водоросли, в самых глубоких — красные, бурые водоросли занимают промежуточное положение. Такое распределение водорослей вызывается следующими причинами. Спектральный состав и интенсивность солнечного света, проходящего через толщу воды, претерпевают большие изменения. Поглощаясь избирательно, солнечный свет обедняется в первую очередь красными лучами, и на глубине в несколько метров он становится синевато-зеленоватым, практически лишенным красных лучей, которые полностью гасятся на глубине примерно 20 м. В связи с этим появление в процессе эволюции дополнительных к хлорофиллу пигментов, интенсивно поглощающих зеленые и желтые лучи, обеспечило красным и бурым водорослям возможность использования для фотосинтеза тех участков солнечного света, которые достигают больших глубин. Можно сказать, что наличие у бурых и красных водорослей дополнительных пигментов следует рассматривать как специальное приспособление к условиям освещения, и в первую очередь как хроматическую адаптацию к наилучшему использованию лучей преобладающей окраски, проходящих через толщу воды.
Кроме того, при прохождении света через толщу воды резко снижается и его интенсивность. Так, свет, проникающий на 20-метровую глубину, ослаблен по сравнению с освещенностью водной поверхности примерно в 20 раз. Поэтому у глубоководных морских водорослей, помимо хроматической адаптации, хорошо выражено также и приспособление к использованию света очень низкой интенсивности. Глубоководные водоросли с полным основанием могут быть отнесены к типичным «тенелюбивым» растениям с высоким содержанием пигментов, в связи с чем прямой солнечный свет повреждает их.
Что касается наземных растений, то у них первостепенное значение имеет адаптация к интенсивности света, поскольку интенсивность света подвержена колебаниям в большей мере, чем его спектральный состав. Хроматическая адаптация выражена у них слабо и проявляется в изменении соотношений между разными пигментами хлоропластов, главным образом между хлорофиллом a и хлорофиллом b, а также между хлорофиллами и каротиноидами.
Адаптация к интенсивности света у наземных растений проявляется в существовании тенелюбивых и светолюбивых типов. У тенелюбивых растений, произрастающих, например, под пологом леса, хорошо выражена адаптация к условиям слабого освещения. Как известно, затененные листья отличаются гораздо более высоким содержанием зеленых пигментов в целом, что содействует лучшему поглощению света низкой интенсивности. Кроме того, листья теневыносливых растений содержат больше хлорофилла Ь, ив этом как раз нетрудно усмотреть приспособление к несколько измененному спектральному составу света, проникающего под полог леса. В тени под нависающей сверху листвой рассеянный свет относительно обогащен коротковолновыми лучами в области 450—480 ∙ 10-9 м, которые интенсивно поглощаются хлорофиллом 6, иногда называемым в связи с этим теневым зеленым пигментом.
Биосинтез пигментов
Исключительно большие успехи достигнуты за последние 20 лет в области изучения биосинтеза пигментов. Особенно глубоко к настоящему времени изучен биосинтез хлорофилла. С помощью меченых атомов, бумажной хроматографии и других современных методов исследования удалось почти полностью расшифровать химизм всех основных этапов формирования молекулы хлорофилла, определить их последовательность, а также выяснить условия, необходимые для протекания тех или иных реакций, и ферментные системы, катализирующие отдельные реакции. Мы не имеем возможности остановиться здесь подробно на всех реакциях биосинтетической цепи хлорофилла, опишем лишь вкратце основные этапы и приведем структурные формулы важнейших промежуточных соединений.
Начальный этап биосинтеза молекулы хлорофилла a включает ряд реакций, в результате которых из несложных органических веществ — аминокислоты гликокола (NH2—СН2—СООН) и янтарной кислоты (НООС—СН2—СН2—СООН) — возникает δ-аминолевулиновая кислота, а при конденсации двух молекул этой кислоты образуется порфобилиноген.
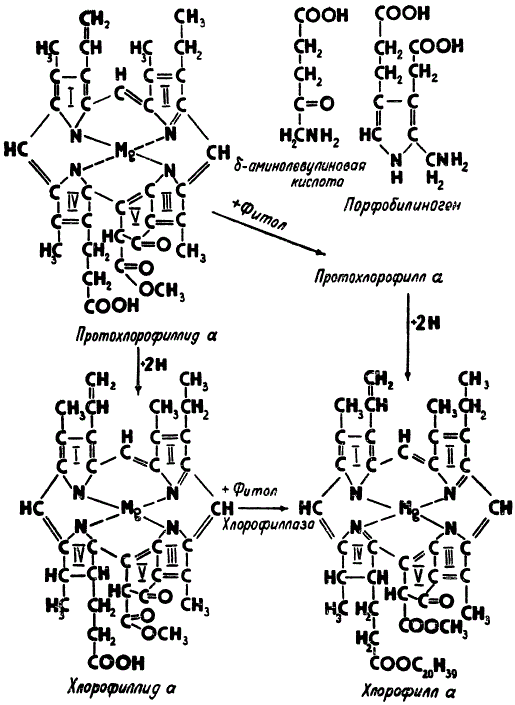
Важнейшие промежуточные соединения биосинтеза хлорофилла а.
Один из следующих важных этапов складывается из реакций, приводящих сначала к синтезу основного структурного ядра хлорофилла путем соединения четырех молекул порфобилиногена, а затем к образованию протохлорофиллида а, имеющего уже в своем составе атом магния. После этого происходит восстановление протохлорофиллида, присоединяющего два атома водорода за счет двойной связи четвертого пиррольного кольца, и превращение его в хлорофиллид а. Для подавляющего большинства видов растений эта реакция является фотохимической и происходит только в присутствии света. Исключение составляют многие водоросли, а также некоторые представители мхов и папоротников, у которых реакция восстановления может осуществляться и в темноте.
У большинства голосеменных растений зеленеть в темноте могут только проростки, если они связаны с эндоспермом.
Вслед за фотохимическим восстановлением имеет место присоединение к хлорофиллиду а фитола, которое не нуждается в присутствии света, но осуществляется при участии фермента хлорофиллазы. Присоединение фитола — это заключительный этап биосинтетической цепи, на котором хлорофиллид а превращается в хлорофилл а.
Раньше считалось, что к протохлорофиллиду сначала присоединяется не водород, а фитол, а затем уже образующийся при этом протохлорофилл восстанавливается фотохимически до хлорофилла. Получалось, что непосредственным предшественником хлорофилла следовало признать протохлорофилл. Сравнительно недавно было установлено, что хотя образование протохлорофилла в растении таким путем и не исключается, однако последний этап биосинтеза хлорофилла осуществляется главным образом через хлорофиллид, который служит основным предшественником хлорофилла.
С помощью меченых атомов показано, что хлорофилл a является в свою очередь предшественником хлорофилла b. При этом одновременно было доказано, что биосинтез хлорофилла b из хлорофилла а не нуждается в обязательном участии света и может происходить даже в полной темноте.
Хлорофилл с может образовываться в растениях, согласно предположению С. Граника, из протохлорофиллида а, поскольку оба эти соединения имеют невосстановленное четвертое пиррольное кольцо и лишены фитольного остатка.
Биосинтез каротиноидов изучен пока недостаточно полно и не все его звенья установлены окончательно. До сих пор не расшифрован химизм отдельных реакций и не выявлена природа соединений, которые служат непосредственными предшественниками различных каротиноидов. Лучше всего изучены начальные этапы, и можно считать окончательно доказанным, что биосинтез каротиноидов и фитола идет одним и тем же путем по крайней мере до образования мевалоновой кислоты.
Установлено также, что свет стимулирует биосинтез как каротиноидов, так и фитола. Хотя образование этих веществ протекает интенсивнее на свету, свет все-таки не обязателен для их биосинтеза. Дальнейшие этапы перехода от мевалоновой кислоты, имеющей в своем составе шесть углеродных атомов, к фитолу, содержащему двадцать углеродных атомов, и тем более к каротиноидам, содержащим сорок углеродных атомов, окончательно еще не установлены и трактуются по-разному.
В ходе исследования биосинтеза зеленых пигментов возникло представление о возможной связи между образованием и разрушением молекул хлорофилла. В дальнейшем с помощью изотопного метода Ф. В. Турчину, В. М. Кутюрину, А. А. Шлыку и другим удалось обнаружить и изучить процесс обновления хлорофилла. По мнению А. А. Шлыка, полученные экспериментальные данные позволяют говорить пока что о главном способе обновления хлорофилла — через распад молекул, ранее образовавшихся, и полный синтез новых. Скорость обновления может изменяться в зависимости как от вида растения, так и от условий произрастания. По предварительным данным, в течение суток обычно обновляется около 10% общего числа всех имеющихся молекул. Однако в некоторых случаях скорость обновления может быть очень низкой, граничащей с полной приостановкой этого процесса.
С помощью изотопного метода выяснена также особая роль только что синтезированных («молодых») молекул в обмене хлорофилла. Особая роль «молодых» молекул обусловлена тем, что они находятся в более реакционноспособном, более лабильном (подвижном) состоянии, чем «старые» молекулы. Причем повышенной лабильностью обладают «молодые» молекулы хлорофилла a и хлорофилла b. Об этом свидетельствуют различия в свойствах «молодых» и «старых» молекул. Например, «молодые» молекулы хлорофилла a легче экстрагируются органическими растворителями, легче теряют окраску и разрушаются при действии кислот, ультразвука или при отсутствии света, а также легче превращаются в хлорофилл b.
Биосинтез пигментов представляет собой цепь процессов, которые протекают не изолированно и самостоятельно, а находятся во взаимосвязи со всем обменом веществ и жизнедеятельностью растительного организма. Большое влияние на биосинтез пигментов оказывает также действие различных факторов внешней среды, в том числе и действие света, о чем говорилось выше. Так, образование хлорофилла возможно только при наличии кислорода в окружающей среде. Отсутствие кислорода тормозит этот процесс, как и понижение температуры. По данным Т. Н. Годнева и его сотрудников, синтез хлорофилла у некоторых вечнозеленых растений может наблюдаться при температуре не ниже —2°, а каротиноидов — не ниже —5°, в то время как способность осуществлять фотосинтез сохраняется у этих видов растений даже при — Небольшое влияние на образование хлорофилла оказывают условия минерального питания. Широко известно явление хлороза у растений (от греч. хлорос — зеленовато-желтый, бледный), когда листья бедны хлорофиллом и имеют желтоватую окраску. Наиболее часто хлороз вызывается отсутствием или недостатком в питательной среде железа, но эта связь наблюдается не всегда. Хлоротичные растения могут развиваться и при недостатке или отсутствии в окружающей среде магния, меди, серы, калия и некоторых других элементов минерального питания. Недостаток калия вызывает хлороз, так же как и избыточные количества этого элемента при недостаточно хорошем азотном питании. При недостатке азота наблюдается резкое ослабление синтеза хлорофилла. Отсутствие или недостаток магния в почве также неизбежно вызывает хлороз растений, поскольку этот элемент входит в состав молекулы хлорофилла.
Значение хлорофилла и каротина для медицины
Хлорофилл и другие пигменты независимо от их роли и значения для фотосинтеза сами по себе являются ценными органическими веществами. Очень важна близость химического состава каротина и витамина А. Каротин можно рассматривать как провитамин А, поскольку при расщеплении его молекулы пополам с присоединением кислорода образуется две молекулы этого витамина. У животных такое расщепление каротина до витамина А происходит при участии особого фермента — каротиназы, который содержится в их печени.
Все более широкое применение в медицине в последнее время находит и хлорофилл. Ценные терапевтические свойства хлорофилла, вероятно, можно объяснить тем, что по своему строению он весьма близок к красящему веществу гемоглобина крови. Поэтому нет ничего неожиданного в том, что в организме человека и животных хлорофилл содействует усиленному образованию гема гемоглобина крови, а также способствует заживлению ран. Кроме того, оказалось, что свойства хлорофилла и витаминов во многом сходны.
Источник: Н.Н. Овчинников, Н.М. Шиханова. Фотосинтез. Пособие для учителей. Изд-во «Просвещение». Москва. 1972
